Reagerer magnesium og kobbersulfat?
Her er hvad der sker:
* magnesium (mg) er mere reaktiv end kobber (CU) . Dette betyder, at magnesium har en stærkere tendens til at miste elektroner og danne positive ioner.
* Når magnesium anbringes i en opløsning af kobbersulfat (cuso₄), donerer magnesiumatomerne elektroner til kobberionerne (Cu²⁺) i opløsningen.
* Dette får kobberionerne til at vinde elektroner og blive neutrale kobberatomer, som derefter udfælder ud af opløsningen som massivt kobber.
* Magnesiumionerne (mg²⁺), der blev dannet under reaktionen, opløses i opløsningen og erstatter kobberionerne.
Den samlede reaktion kan repræsenteres af følgende ligning:
MG (S) + CUSO₄ (AQ) → MGSO₄ (AQ) + CU (S)
Observationer:
* Du vil bemærke, at der dannes en rødbrun fast (kobber), der dannes på overfladen af magnesiummetal.
* Den blå farve på kobbersulfatopløsningen falder gradvist, når kobberionerne forbruges.
Vigtig note: Denne reaktion er eksoterm, hvilket betyder, at den frigiver varme. Reaktionsfartøjet kan føles varmt at røre ved.
Sidste artikelEr CH4 en fed eller olie?
Næste artikelEr smeltning af en fed kemisk ændring?
 Varme artikler
Varme artikler
-
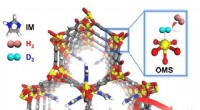 Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen
Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen -
 At finde nyt liv til vin-drue-resterKredit:CC0 Public Domain Californien producerer næsten 4 millioner tons vin i verdensklasse hvert år, men med det kommer tusindvis af tons af rester som drueskind, frø, stængler og frugtkød. Hvad
At finde nyt liv til vin-drue-resterKredit:CC0 Public Domain Californien producerer næsten 4 millioner tons vin i verdensklasse hvert år, men med det kommer tusindvis af tons af rester som drueskind, frø, stængler og frugtkød. Hvad -
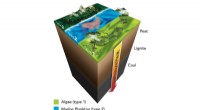 Forskere bruger røntgenstråler til at knække skiferens hemmeligheder, en hjørnesten i en af na…Som vist i denne illustration, som kulstof som det der findes i alger, marine plankton og kystnære landplanter bevæger sig tættere på Jordens kerne, det udsættes for højere temperaturer og tryk, der æ
Forskere bruger røntgenstråler til at knække skiferens hemmeligheder, en hjørnesten i en af na…Som vist i denne illustration, som kulstof som det der findes i alger, marine plankton og kystnære landplanter bevæger sig tættere på Jordens kerne, det udsættes for højere temperaturer og tryk, der æ -
 Kan en højteknologisk sniffer hjælpe med at holde os sikre?NIST -kemiker Megan Harries tester, om en bærbar, højteknologisk sniffeanordning kaldet et PLOT-cryo-system kan bruges til at afskærme forsendelsescontainere for farlige luftbårne kemikalier ved indga
Kan en højteknologisk sniffer hjælpe med at holde os sikre?NIST -kemiker Megan Harries tester, om en bærbar, højteknologisk sniffeanordning kaldet et PLOT-cryo-system kan bruges til at afskærme forsendelsescontainere for farlige luftbårne kemikalier ved indga
- Hvad er de operationelle definitioner for kuldioxid?
- Mnyamawamtuka:Ny dinosaur med hjerteformet hale giver evolutionære spor for det afrikanske kontinen…
- Hvad bruges fossiler til at bestemme de relative aldre af klippelag?
- Var Mercury 1 den første NASA -mission?
- Bolivia har mistet 1,7 millioner hektar til brand:regeringen
- En carboxylsyre, der har en lang carbonhydridkæde og afledt af naturlig kilde.?


