Kemisk basics af brintbinding og proteiner?
Kemisk basics af brintbindinger og proteiner:
Hydrogenbinding:
En hydrogenbinding er en speciel type dipol-dipolinteraktion, der forekommer mellem et hydrogenatom kovalent bundet til et stærkt elektronegativt atom (som ilt, nitrogen eller fluor) og et elektronpar af et andet elektronegativt atom.
Nøglefunktioner:
* stærkeste dipol-dipolinteraktion: Det er stærkere end typiske dipol-dipolinteraktioner på grund af den høje elektronegativitetsforskel mellem hydrogenatomet og det elektronegative atom, det er bundet til.
* svag sammenlignet med kovalente obligationer: Mens der er stærkere end typiske dipol-dipol-interaktioner, er hydrogenbindinger stadig svagere end kovalente bindinger.
* retningsbestemt: Bindingen er retningsbestemt, hvilket betyder, at den dannes i en bestemt orientering.
* Vigtigt for biologiske systemer: Hydrogenbindinger spiller en afgørende rolle i at holde biologiske molekyler sammen med DNA, RNA og proteiner.
Proteiner:
Proteiner er store, komplekse biomolekyler, der er essentielle for forskellige biologiske funktioner. De består af kæder af aminosyrer forbundet med peptidbindinger.
Rollen af brintbindinger i proteiner:
Hydrogenbindinger spiller en afgørende rolle i bestemmelsen af strukturen og funktionen af proteiner. De er involveret i:
* Sekundær struktur:
* α-helix: Hydrogenbindinger dannes mellem carbonylgruppen af en aminosyre og amidhydrogenet af en aminosyre fire rester foran i kæden og danner en spiralformet struktur.
* β-ark: Hydrogenbindinger dannes mellem tilstødende polypeptidkæder og holder dem sammen i en arklignende struktur.
* tertiær struktur: Interaktioner mellem sidekæder af aminosyrer, herunder brintbindinger, bidrager til den samlede tredimensionelle foldning af proteinet.
* kvartær struktur: Hydrogenbindinger kan også indeholde flere proteinunderenheder til dannelse af et funktionelt proteinkompleks.
* stabilitet og funktion: Hydrogenbindinger bidrager til stabiliteten af proteinstrukturen og forhindrer den i at udfolde sig. De spiller også en rolle i protein-protein-interaktioner, enzym-substratinteraktioner og andre vigtige biologiske processer.
Specifikke eksempler:
* DNA: Hydrogenbindinger holder de to DNA -tråde, hvilket muliggør nøjagtig replikation og transkription af genetisk information.
* Vand: Vandmolekyler danner brintbindinger med hinanden, hvilket giver vand sine unikke egenskaber som højt kogepunkt og overfladespænding.
Kortfattet:
Hydrogenbindinger er grundlæggende kræfter, der påvirker strukturen og funktionen af proteiner. De er afgørende for at opretholde stabiliteten af proteinstrukturen, muliggøre korrekt foldning og lette protein-proteininteraktioner. De er også involveret i mange andre biologiske processer og fremhæver deres betydning i livet.
 Varme artikler
Varme artikler
-
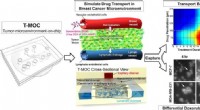 Mikrofluidisk anordning simulerer kræftbehandling lige så effektivt som forskningsdyrDenne grafik viser, hvordan en ny teknologi udviklet på Purdue University, der simulerer tumorer. Kredit:Purdue University foto/Altug Ozcelikkale En ny teknologi, der simulerer tumorer, har vist s
Mikrofluidisk anordning simulerer kræftbehandling lige så effektivt som forskningsdyrDenne grafik viser, hvordan en ny teknologi udviklet på Purdue University, der simulerer tumorer. Kredit:Purdue University foto/Altug Ozcelikkale En ny teknologi, der simulerer tumorer, har vist s -
 Cellemembran som materiale til knogledannelseForståelse af biologiske fænomener fra en tværfaglig tilgang muliggør udvikling og optimering af bioinspirerede materialer. Kredit:Bioinspired Engineering Udbruddet af celler, der danner brusk, er
Cellemembran som materiale til knogledannelseForståelse af biologiske fænomener fra en tværfaglig tilgang muliggør udvikling og optimering af bioinspirerede materialer. Kredit:Bioinspired Engineering Udbruddet af celler, der danner brusk, er -
 Fremstilling af etan fra metan ved hjælp af en fotokemisk looping -strategiÆndringer af Ag – HPW/TiO 2 efter metan fotokemisk kobling. Kredit: Naturenergi (2020). DOI:10.1038/s41560-020-0616-7 Et team af forskere fra universitetet i Lille, CNRS, Centrale Lille, Univer
Fremstilling af etan fra metan ved hjælp af en fotokemisk looping -strategiÆndringer af Ag – HPW/TiO 2 efter metan fotokemisk kobling. Kredit: Naturenergi (2020). DOI:10.1038/s41560-020-0616-7 Et team af forskere fra universitetet i Lille, CNRS, Centrale Lille, Univer -
 Hvorfor bioelektroder til energiomdannelse ikke er stabileFelipe Conzuelo og Fangyuan Zhao har undersøgt, hvorfor kunstige fotosyntesesystemer er ustabile. Kredit:RUB, Kramer Forskere ved Ruhr-Universität Bochum har opdaget, hvorfor bioelektroder, der in
Hvorfor bioelektroder til energiomdannelse ikke er stabileFelipe Conzuelo og Fangyuan Zhao har undersøgt, hvorfor kunstige fotosyntesesystemer er ustabile. Kredit:RUB, Kramer Forskere ved Ruhr-Universität Bochum har opdaget, hvorfor bioelektroder, der in


