Hvad var Ernest Rutherford bidrag til atomet?
* forudgående model: Før Rutherford var den herskende model for atomet "blomme budding -modellen" foreslået af J.J. Thomson. Denne model afbildede atomet som en sfære med positiv ladning med negativt ladede elektroner indlejret i den, som blommer i en budding.
* eksperimentet: Rutherfords team bombarderede et tyndt ark guldfolie med alfa -partikler (positivt ladede partikler). De forventede, at alfa -partiklerne ville passere lige gennem folien, lidt afbøjet højst, baseret på blommepudding -modellen.
* de uventede resultater: Til deres forbløffelse blev en lille procentdel af alfa -partiklerne afbøjet i store vinkler, nogle hoppede endda tilbage! Dette var en revolutionær konstatering.
* Rutherfords fortolkning: Rutherford fortolkede disse resultater som følger:
* Atomet indeholder en lille, tæt, positivt ladet kerne i midten.
* De negativt ladede elektroner kredser om kernen som planeter omkring solen.
* Rutherford -modellen: Denne model, kendt som nuklear model , revolutionerede vores forståelse af atomet. Det var langt fra blommepudding -modellen og lagde grundlaget for fremtidige atommodeller som Bohrs model.
Rutherfords eksperiment og hans model viste, at:
* Atomer er ikke solide kugler, men har en central kerne.
* Kernen er positivt ladet og indeholder det meste af atomets masse.
* Elektroner optager et stort rum omkring kernen og kredserer den i en skylignende struktur.
Hans opdagelse åbnede nye muligheder for forskning inden for nuklear fysik og førte til udviklingen af atomenergi og andre teknologier.
 Varme artikler
Varme artikler
-
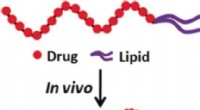 Transport af lipidkonjugeret floxuridin med naturligt serumalbumin til levering til kræftcellerKredit:Wiley Hvordan kan eliminering af terapeutiske midler fra blodbanen eller deres tidlige enzymatiske nedbrydning undgås ved systemisk levering? Kinesiske forskere har nyudviklet en metode til
Transport af lipidkonjugeret floxuridin med naturligt serumalbumin til levering til kræftcellerKredit:Wiley Hvordan kan eliminering af terapeutiske midler fra blodbanen eller deres tidlige enzymatiske nedbrydning undgås ved systemisk levering? Kinesiske forskere har nyudviklet en metode til -
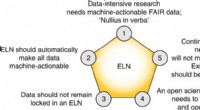 Kemisk datahåndtering:En åben vej fremDe fem kerneteser i dette perspektiv. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00910-7 Et af de mest udfordrende aspekter af moderne kemi er håndtering af data. For eksempel, når de s
Kemisk datahåndtering:En åben vej fremDe fem kerneteser i dette perspektiv. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00910-7 Et af de mest udfordrende aspekter af moderne kemi er håndtering af data. For eksempel, når de s -
 Forskning kan hjælpe fleksibel teknologi til at vare længere, undgå kritiske fejlGuy German er lektor i biomedicinsk teknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Uanset om det er ved regelmæssig brug
Forskning kan hjælpe fleksibel teknologi til at vare længere, undgå kritiske fejlGuy German er lektor i biomedicinsk teknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Uanset om det er ved regelmæssig brug -
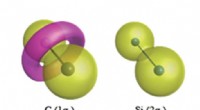 Kerneelektrontopologier i kemisk bindingIndre kerneelektroner forventes at have en jordnøddelignende bølgefunktion som vist for Si 2 s elektroner (højre). I C-C-bindingen, imidlertid, C1s-elektronerne danner et torus-lignende træk med mod
Kerneelektrontopologier i kemisk bindingIndre kerneelektroner forventes at have en jordnøddelignende bølgefunktion som vist for Si 2 s elektroner (højre). I C-C-bindingen, imidlertid, C1s-elektronerne danner et torus-lignende træk med mod
- Fukushima-katastrofe:Vigtige takeaways 8 år senere
- Intensivering af landbruget og sociale hierarkier udvikler sig sammen, undersøgelse finder
- Er fodbiotisk eller abioitisk?
- Hvilken ændring i en Stars -egenskaber ville indikere, at den begynder at dø?
- Hvor ofte sker der tornadoer og orkaner i den tempererede regnskov?
- Uddybende spørgsmål:Hvad forudsiger et lykkeligt ægteskab?


