Når Chemical X reduceres, hvilken af disse udtryk, der ville være en nøjagtig repræsentation, dens tilstand?
Forståelse af reduktion
* Gevinst af elektroner: Reduktion er en kemisk proces, hvor et stof får elektroner. Dette fører ofte til et fald i stoffets oxidationstilstand.
* ændret ansvar: Gevinsten af elektroner kan ændre det samlede ladning af stoffet.
Repræsenterer staten
Sådan repræsenterer du muligvis den reducerede tilstand af kemisk x, afhængigt af detaljerne:
* Kemisk formel:
* Hvis X er en simpel ion, ændres dens ladning. For eksempel, hvis X starter som Fe³⁺ (jernion med en +3 ladning), kan det reduceres til Fe²⁺.
* Hvis X er en del af en forbindelse, kan den samlede ladning ændre sig, eller oxidationstilstanden for et specifikt atom inden for forbindelsesændringerne. For eksempel kunne CuO (kobberoxid) reduceres til Cu₂o (kobber (I) oxid).
* Oxidationstilstand:
* Oxidationstilstanden af X vil blive mere negativ (eller mindre positiv) efter reduktion. For eksempel, hvis X starter med en oxidationstilstand på +5, kan den reduceres til en oxidationstilstand på +3.
* halvreaktion:
* Du kan skrive en halvreaktion for at repræsentere reduktionsprocessen. Dette viser de opnåede elektroner:
X + ne⁻ → x⁻ⁿ (hvor 'n' repræsenterer antallet af opnåede elektroner)
har brug for mere information
For at give dig en præcis repræsentation, skulle jeg vide:
* Starttilstanden for kemisk x: Hvad er dens kemiske formel, ladning eller oxidationstilstand?
* Den specifikke reduktionsproces: Hvad forårsager reduktionen?
Fortæl mig, om du kan give flere detaljer om kemisk X og reduktionsprocessen, og jeg kan give dig en mere nøjagtig repræsentation!
 Varme artikler
Varme artikler
-
 At gøre alkohol til nøgleingredienser til ny medicinForskere har fundet en måde at omdanne alkohol til aminosyrer, afgørende komponenter i mange lægemidler. Kredit:Unsplash Kemikere har fundet en måde at omdanne alkohol til aminosyrer, livets bygge
At gøre alkohol til nøgleingredienser til ny medicinForskere har fundet en måde at omdanne alkohol til aminosyrer, afgørende komponenter i mange lægemidler. Kredit:Unsplash Kemikere har fundet en måde at omdanne alkohol til aminosyrer, livets bygge -
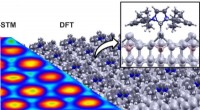 Ny metode til molekylær funktionalisering af overfladerSammenligning af den teoretisk beregnede struktur (DFT, til højre) af det bestilte NHC -enkeltlag med det eksperimentelle scanningstunnelmikroskopibillede (STM, venstre). N:nitrogenatom, C:carbonatom,
Ny metode til molekylær funktionalisering af overfladerSammenligning af den teoretisk beregnede struktur (DFT, til højre) af det bestilte NHC -enkeltlag med det eksperimentelle scanningstunnelmikroskopibillede (STM, venstre). N:nitrogenatom, C:carbonatom, -
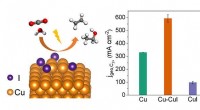 Ny katalysator øger kuldioxid elektroreduktion til multicarbon-produkterEn Cu-CuI-kompositkatalysator opnår højeffektiv produktion af C 2 + kemikalier fra elektrokatalytisk CO 2 reduktion. Kredit:LI Hefei og LIU Tianfu Elektrokatalytisk CO 2 reduktionsreaktion
Ny katalysator øger kuldioxid elektroreduktion til multicarbon-produkterEn Cu-CuI-kompositkatalysator opnår højeffektiv produktion af C 2 + kemikalier fra elektrokatalytisk CO 2 reduktion. Kredit:LI Hefei og LIU Tianfu Elektrokatalytisk CO 2 reduktionsreaktion -
 Forlænger levetiden for polymerelektrolytbrændselsceller med en nanodisperseret ionomerSkema af Nafion-ionomerer på katalysatoroverfladerne. (A) Fordeling af konventionelle ionomerer syntetiseret ved emulsionspolymerisation. (B) Fordeling af laboratoriefremstillede ionomerer syntetisere
Forlænger levetiden for polymerelektrolytbrændselsceller med en nanodisperseret ionomerSkema af Nafion-ionomerer på katalysatoroverfladerne. (A) Fordeling af konventionelle ionomerer syntetiseret ved emulsionspolymerisation. (B) Fordeling af laboratoriefremstillede ionomerer syntetisere
- Oversvømmelse forårsaget af gamle data
- Slæber antiprotoner rundt i en varevogn
- Er nitrogen et metal ikke -metal eller metalloid?
- Hvor sker det meste af erosionen langs denne kystlinje punkt A eller B?
- Mød den lærde, der diagnosticerede overvågningskapitalisme
- Sådan Faktor Polynomier i Faktor Fire Vilkår


