Hvad er forskel mellem fysisk og kemisk balance?
Fysisk vs kemisk balance:En klar sondring
Mens både fysisk og kemisk balance er vigtige koncepter, adskiller de sig i deres grundlæggende karakter og anvendelse:
Fysisk balance:
* fokus: Beskæftiger sig med distribution af masse inden for et system.
* Ændringer: Involverer fysiske transformationer som ændringer i tilstand (fast, flydende, gas), form eller størrelse.
* Eksempler:
* en seesaw: Afbalanceret, når vægte på begge sider er ens.
* En løsning: Når opløsning er jævnt fordelt over opløsningsmidlet.
* en kemisk reaktion: Når hastigheden af fremad- og omvendt reaktioner er ens, hvilket resulterer i en konstant koncentration af reaktanter og produkter (dynamisk ligevægt).
* Nøglepunkt: Ingen nye stoffer dannes , kun arrangementet eller distributionen af eksisterende stoffer ændres.
Kemisk balance:
* fokus: Beskæftiger sig med nummer og typer atomer involveret i en kemisk reaktion.
* Ændringer: Involverer kemiske reaktioner hvor atomer omarrangeres til dannelse af nye molekyler.
* Eksempler:
* en kemisk ligning: Afbalanceret, når antallet af atomer i hvert element på reaktantsiden er lig med antallet på produktsiden.
* En forbrændingsreaktion: Hvor brændstof og ilt reagerer på dannelse af kuldioxid og vand, hvilket sikrer, at alle atomer er redegjort for.
* Nøglepunkt: nye stoffer dannes med forskellige egenskaber end de originale reaktanter.
i enklere termer:
* Fysisk balance: Som en seesaw, hvor lige vægte på begge sider skaber stabilitet.
* Kemisk balance: Som en opskrift, hvor alle ingredienser bruges og intet er tilbage.
Her er en tabel, der opsummerer de vigtigste forskelle:
| Funktion | Fysisk balance | Kemisk balance |
| --- | --- | --- |
| Fokus | Massefordeling | Atomtælling og type |
| Ændringer | Fysiske transformationer | Kemiske reaktioner |
| Nøglepunkt | Ingen nye stoffer dannet | Nye stoffer dannet |
Konklusion:
At forstå både fysisk og kemisk balance er afgørende inden for forskellige områder, herunder kemi, fysik og teknik. De hjælper os med at forudsige, hvordan systemer vil opføre sig og sikre sikre og effektive processer.
 Varme artikler
Varme artikler
-
 Ny syntetisk rute til produktion af biobrændstofferDet Bochum-baserede katalyseteam:Baoxiang Peng (til venstre) og Martin Muhler. Kredit:RUB, Rohlf Et tysk-kinesisk forskerhold har fundet en ny syntetisk rute til fremstilling af biobrændstof fra b
Ny syntetisk rute til produktion af biobrændstofferDet Bochum-baserede katalyseteam:Baoxiang Peng (til venstre) og Martin Muhler. Kredit:RUB, Rohlf Et tysk-kinesisk forskerhold har fundet en ny syntetisk rute til fremstilling af biobrændstof fra b -
 Tre forskere vinder Nobelprisen i kemi for udviklingen inden for elektronmikroskopiEn revolutionerende teknik kaldet kryo-elektronmikroskopi, som har set nærmere på Zika -viruset og et Alzheimers enzym, tjente forskere Jacques Dubochet, Joachim Frank og Richard Henderson Nobels kemi
Tre forskere vinder Nobelprisen i kemi for udviklingen inden for elektronmikroskopiEn revolutionerende teknik kaldet kryo-elektronmikroskopi, som har set nærmere på Zika -viruset og et Alzheimers enzym, tjente forskere Jacques Dubochet, Joachim Frank og Richard Henderson Nobels kemi -
 Ultralydsenhed forbedrer opladningstiden og driftstiden i lithiumbatterierEnheden er lavet af hylde-smartphone-komponenter, som genererer lydbølger ved ekstremt høje frekvenser - fra 100 millioner til 10 milliarder hertz. I telefoner, disse enheder bruges hovedsageligt til
Ultralydsenhed forbedrer opladningstiden og driftstiden i lithiumbatterierEnheden er lavet af hylde-smartphone-komponenter, som genererer lydbølger ved ekstremt høje frekvenser - fra 100 millioner til 10 milliarder hertz. I telefoner, disse enheder bruges hovedsageligt til -
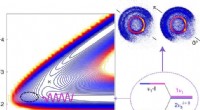 Brug af kvantevibrationsegenskaber mellem molekyler til at fremskynde reaktioner mellem forbindelserGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00914-3 Et par forskere, den ene med Southern University of Science and Technology, den anden Institute of Atomic and Molecu
Brug af kvantevibrationsegenskaber mellem molekyler til at fremskynde reaktioner mellem forbindelserGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00914-3 Et par forskere, den ene med Southern University of Science and Technology, den anden Institute of Atomic and Molecu
- Billede:Påvirkning af en solstorm, 28. oktober 2003
- Hvilken reaktion producerer saccharose fra glucose og fruktose?
- Hvad er kilden til mørke og koldt siden solvarmlys?
- Mobiltelefoner vinder accept i amerikanske skoler
- Hvad er kosmiders rolle i den rekombinent DNA -teknologi?
- Antropologers forskning kaster lys over den voksende befolkning af ikke-religiøse marokkanere


