Hvis elektronens energi i jordtilstand er et hydrogenatom 1 Rydberg, så så ville det være at Z svarer til 4?
Forståelse af Rydbergs formel
Rydbergs formel giver energiniveauet for et elektron i et brintlignende atom:
E =-13.6 * (Z^2 / N^2) EV
Hvor:
* e er elektronens energi (i elektron volt, EV)
* z er atomnummeret (antal protoner)
* n er det vigtigste kvantetal (1 for jordtilstanden)
Anvendelse af formlen
1.. z =4: Dette betyder, at vi har at gøre med et atom med 4 protoner (som beryllium).
2. n =1: Vi er interesseret i jordtilstanden, så det vigtigste kvantetal er 1.
Tilslutning af disse værdier til formlen:
E =-13.6 * (4^2/1^2) EV
E =-13,6 * 16 eV
E =-217.6 eV
svaret
Elektronens energi i jordtilstanden for et brintlignende atom med Z =4 er -217,6 eV.
Vigtig note: Dette er energien i forhold til den ioniserede tilstand (når elektronet fjernes fuldstændigt fra atomet). Energien er negativ, fordi elektronet er bundet til kernen.
 Varme artikler
Varme artikler
-
 Blistervæske kan hjælpe med at diagnosticere forbrændingens sværhedsgradKredit:American Chemical Society Alvorlige forbrændinger kan efterlade fysiske og psykiske ar, især hos børn. Når en forbrændingspatient kommer ind på klinikken, læger bruger faktorer som forbrænd
Blistervæske kan hjælpe med at diagnosticere forbrændingens sværhedsgradKredit:American Chemical Society Alvorlige forbrændinger kan efterlade fysiske og psykiske ar, især hos børn. Når en forbrændingspatient kommer ind på klinikken, læger bruger faktorer som forbrænd -
 Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h
Hamp testlaboratorium lanceret som svar på industriens behovChristopher Perkins 89 (CAHNR) 95 MS, anbringer bakker med hamp i en tørremaskine på UConns Center for Environmental Sciences and Engineering laboratorium. Kredit:Sean Flynn/UConn Som svar på en h -
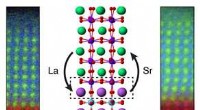 Udnyttelse af tabte atomer kan hjælpe med at skabe nye, aldrig før sete oxiderKemisk kortlægning og illustration af atomare omlejring ved grænsefladen mellem to oxidmaterialer (La =lanthan; Sr =strontium). Kredit:PNNL At forstå, hvordan materialer dannes og kombineres med h
Udnyttelse af tabte atomer kan hjælpe med at skabe nye, aldrig før sete oxiderKemisk kortlægning og illustration af atomare omlejring ved grænsefladen mellem to oxidmaterialer (La =lanthan; Sr =strontium). Kredit:PNNL At forstå, hvordan materialer dannes og kombineres med h -
 Mellemlag hjælper perovskitkrystallisering til højtydende lysemitterende dioderForskellige metaloxidlag påvirker egenskaberne af de tynde perovskitfilm. Kredit:Charlotte Perhammar Forskere ved LiU, der arbejder med kolleger fra Kina, har vist, hvordan man opnår effektive per
Mellemlag hjælper perovskitkrystallisering til højtydende lysemitterende dioderForskellige metaloxidlag påvirker egenskaberne af de tynde perovskitfilm. Kredit:Charlotte Perhammar Forskere ved LiU, der arbejder med kolleger fra Kina, har vist, hvordan man opnår effektive per
- Hvad vi ved om orkanen Irma:fakta, tal, prognose
- Kan en vandrum udgøre en tornado?
- Ionisk defekt landskab i perovskit solceller afsløret
- Kvantitativ 3D-analyse af knogleværktøjer kaster lys over gammel fremstilling og brug
- Hvad er oprindelsen af en jernmeteorit?
- Forbudte urter? Virkningerne af cannabis var et kontroversielt emne for 250 år siden


