Hvad viser ændringer, der finder sted under en kemisk reaktion?
observerbare ændringer:
* farveændring: En ændring i reaktanternes farve eller udseendet af en ny farve.
* Dannelse af et bundfald: Dannelsen af et fast stof, der sætter sig ud af en opløsning.
* Gasudvikling: Produktionen af bobler, der angiver dannelsen af en gas.
* Temperaturændring: Reaktionen kan frigive varme (eksotermisk) eller absorbere varme (endotermisk), hvilket forårsager en ændring i temperaturen.
* Lysemission: Nogle kemiske reaktioner producerer lys, som i en ildflug eller glødestok.
* Ændring i lugt: En ny eller anden lugt kan indikere, at der er dannet et nyt stof.
mindre indlysende ændringer:
* Ændring i kemisk sammensætning: Dette er den grundlæggende ændring i en kemisk reaktion. Nye stoffer dannes med forskellige kemiske bindinger og egenskaber.
* Ændring i pH: Dette er et mål for surhed eller alkalinitet og kan ændre sig, når der dannes nye stoffer.
* Ændring i elektrisk ledningsevne: Dette kan måles for at bestemme, om ioner er til stede, hvilket kan dannes under en reaktion.
Vigtig note: Ikke alle disse ændringer vil være til stede i enhver kemisk reaktion. Nogle reaktioner viser muligvis kun en subtil ændring i kemisk sammensætning, mens andre kan ledsages af flere dramatiske ændringer.
værktøjer til at registrere forandring:
* spektrofotometer: Måler lysabsorption og transmission, som kan identificere specifikke stoffer.
* kromatografi: Adskiller blandinger, hvilket tillader identifikation af individuelle komponenter.
* pH -meter: Måler surhedsgrad eller alkalinitet.
* termometer: Måler temperaturændringer.
Ved at observere disse ændringer og bruge specialiserede værktøjer kan forskere forstå de komplekse transformationer, der forekommer under kemiske reaktioner.
Sidste artikelSom alle materie er mineraler lavet af?
Næste artikelHvor mange hydrogenatomer har cyclohexan?
 Varme artikler
Varme artikler
-
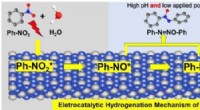 Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly
Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly -
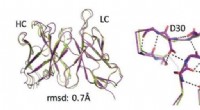 Principper for beregningsmæssigt design af bindende antistofferComputerdesign (limegrøn) sammenlignes med eksperimentelle strukturer (lilla) på atomniveau, afslører atomnøjagtighed i overordnet struktur (venstre) og i sløjfeområder (højre). Kredit:Weizmann Instit
Principper for beregningsmæssigt design af bindende antistofferComputerdesign (limegrøn) sammenlignes med eksperimentelle strukturer (lilla) på atomniveau, afslører atomnøjagtighed i overordnet struktur (venstre) og i sløjfeområder (højre). Kredit:Weizmann Instit -
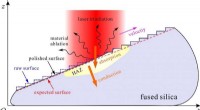 CO2 -laserablation fører en ny vej til skræddersyede kontinuerlige smeltede silicaoverfladerFigur 1. Skematisk diagram for 2-D numerisk model af CO 2 laserablation. Kredit:SIOM Smeltet silica er et vigtigt materiale til mange anvendelser inden for optik og fotonik på grund af dets frem
CO2 -laserablation fører en ny vej til skræddersyede kontinuerlige smeltede silicaoverfladerFigur 1. Skematisk diagram for 2-D numerisk model af CO 2 laserablation. Kredit:SIOM Smeltet silica er et vigtigt materiale til mange anvendelser inden for optik og fotonik på grund af dets frem -
 Botulinum-type toksiner springer til en ny slags bakterierUdseendet af et botulinumlignende toksin i Enterococcus -en allestedsnærværende bakterie og en fremvoksende årsag til multiresistente infektioner-vækker videnskabelig bekymring. Kredit:Francois Lebr
Botulinum-type toksiner springer til en ny slags bakterierUdseendet af et botulinumlignende toksin i Enterococcus -en allestedsnærværende bakterie og en fremvoksende årsag til multiresistente infektioner-vækker videnskabelig bekymring. Kredit:Francois Lebr
- Mod byluftmobilitet:Lufttaxier med side-by-side rotorer
- Maskinlæring afslører skjult skildpaddemønster i kvantefyrværkeri
- Hvordan insekter kontrollerer deres vinger:Insektflugtens mystiske mekanik
- Hvad kaldes en kovalent binding, hvor elektroner deles ligeligt?
- Sådan beregnes plasma Osmolarity
- En blød fototaktisk svømmerobot bygget ved hjælp af en selvforsynende hydrogeloscillator


