Den molekylære formel til hydratiseret silica?
Her er hvorfor:
* Silica (SiO2) er et netværksstof: Dets struktur er et enormt, tredimensionelt netværk af silicium- og iltatomer.
* Hydrering: Vandmolekyler kan absorberes fysisk på silicaoverfladen eller er kemisk bundet til silica -strukturen gennem brintbinding.
* Variabelt vandindhold: Mængden af vandmolekyler, der er forbundet med silica, kan variere meget, hvilket fører til forskellige former og egenskaber.
Her er nogle eksempler:
* silicagel: En almindelig form for hydreret silica med et højt overfladeareal anvendt som et tørremiddel (tørringsmiddel). Det har ikke en defineret kemisk formel, men har typisk et vandindhold på ca. 5-15%.
* opal: En smuk ædelsten, der i det væsentlige er hydreret silica med et højt vandindhold (ca. 5-20%). Dens specifikke formel afhænger af den nøjagtige mængde vand.
* Andre hydratiserede silicater: Forskellige andre silikater med forskellige vandindhold, inklusive lermineraler, betragtes også som hydratiseret silica.
For nøjagtigt at repræsentere en hydreret silicaforbindelse skal du specificere den nøjagtige mængde vandmolekyler, der er forbundet med silica. Dette kan gøres ved hjælp af en kemisk formel som:
* siO2 • NH2O
Hvor 'n' repræsenterer antallet af vandmolekyler pr. Silica -molekyle.
Husk, at hydreret silica ikke er en enkelt forbindelse, men en række materialer med forskellige vandindhold og egenskaber.
Sidste artikelNår fossile brændstoffer brænder, hvad er reaktanterne?
Næste artikelSO2 er et element eller en forbindelse?
 Varme artikler
Varme artikler
-
 Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m
Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m -
 Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM
Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM -
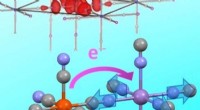 Ultrahurtig ladningsoverførsel i preussisk blå analogerKredit:Wiley Fotoinducerede ladningsoverførsler er en interessant elektronisk egenskab ved preussisk blå og nogle analogt strukturerede forbindelser. Et team af forskere har nu været i stand til a
Ultrahurtig ladningsoverførsel i preussisk blå analogerKredit:Wiley Fotoinducerede ladningsoverførsler er en interessant elektronisk egenskab ved preussisk blå og nogle analogt strukturerede forbindelser. Et team af forskere har nu været i stand til a -
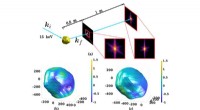 Ny beregningsteknik løser komprimerede røntgendataSkematisk (øverst) viser Braggs kohærente diffraktionsbilleddannelsesfaseindhentning af røntgenstråler spredt af en guldnanopartikel. To rekonstruktioner af guldnanopartiklen er vist forneden. Kredit:
Ny beregningsteknik løser komprimerede røntgendataSkematisk (øverst) viser Braggs kohærente diffraktionsbilleddannelsesfaseindhentning af røntgenstråler spredt af en guldnanopartikel. To rekonstruktioner af guldnanopartiklen er vist forneden. Kredit:
- Rige nationer kommer til kort med løfter om klimafinansiering
- Hvor mange CM er i 568 mm og viser arbejde?
- Hvad er skolernes fysiske ressourcer?
- Forholdet mellem sangrækkefølge og rytmisk timing hos sangfugle
- Apple-konkurrent baner vejen for forbud mod nogle iPhones i Tyskland
- DNA-baseret metode detekterer spormængder af jordnødder i fødevarer


