Bestem den molekylære formel for en forbindelse, hvis dens empiriske er C2H6O og molmasse 138G?
1. Find den empiriske formelmasse:
* C:12,01 g/mol * 2 =24,02 g/mol
* H:1,01 g/mol * 6 =6,06 g/mol
* O:16,00 g/mol * 1 =16,00 g/mol
* Samlet empirisk formelmasse =24,02 + 6,06 + 16,00 =46,08 g/mol
2. Bestem forholdet mellem molekylmasse og empirisk formelmasse:
* Forhold =138 g/mol/46,08 g/mol =3
3. Multiplicer underskrifterne i den empiriske formel med forholdet:
* C2H6O * 3 = C6H18O3
Derfor er den molekylære formel for forbindelsen C6H18O3.
Sidste artikelHvad er chloriner naturlig tilstand?
Næste artikelEr det reversibelt, når eddike opdages på kridt eller kalksten?
 Varme artikler
Varme artikler
-
 Hvad gør den dødbringende pufferfish så lifligForskere har identificeret de vigtigste forbindelser, der er ansvarlige for smagen af pufferfish ( Takifugu obscurus ). Kredit:Yuan Liu Nogle mennesker overvejer pufferfish, også kendt som fug
Hvad gør den dødbringende pufferfish så lifligForskere har identificeret de vigtigste forbindelser, der er ansvarlige for smagen af pufferfish ( Takifugu obscurus ). Kredit:Yuan Liu Nogle mennesker overvejer pufferfish, også kendt som fug -
 Nye molekyler kan bruges til at behandle autoimmune sygdomme i fremtidenKredit:Bart van Overbeeke Når noget er galt med dit immunsystem, din fordøjelse eller dine endokrine systemer nukleare receptorer, som de kaldes, godt kan være involveret. Hvis det er nødvendigt,
Nye molekyler kan bruges til at behandle autoimmune sygdomme i fremtidenKredit:Bart van Overbeeke Når noget er galt med dit immunsystem, din fordøjelse eller dine endokrine systemer nukleare receptorer, som de kaldes, godt kan være involveret. Hvis det er nødvendigt, -
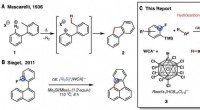 Funktionalisering af uaktiverede alkaner ved hjælp af reaktioner baseret på katalysatorer fremstil…Reaktioner, der involverer formodede phenylkationer. (A) Mascarellis reaktion (12). (B) Siegels intramolekylære Friedel-Crafts reaktion af arylfluorider (15). (C) Vores dobbelte C–F/C–H-funktionaliser
Funktionalisering af uaktiverede alkaner ved hjælp af reaktioner baseret på katalysatorer fremstil…Reaktioner, der involverer formodede phenylkationer. (A) Mascarellis reaktion (12). (B) Siegels intramolekylære Friedel-Crafts reaktion af arylfluorider (15). (C) Vores dobbelte C–F/C–H-funktionaliser -
 Hurtig måling af aerosolens volatilitet ved hjælp af et deep learning-baseret bærbart mikroskopEn mobil og omkostningseffektiv enhed er designet til at måle flygtigheden af partikler ved hjælp af deep learning. Kredit:Ozcan Lab, UCLA. Eksponering for partikler (PM) har været forbundet med
Hurtig måling af aerosolens volatilitet ved hjælp af et deep learning-baseret bærbart mikroskopEn mobil og omkostningseffektiv enhed er designet til at måle flygtigheden af partikler ved hjælp af deep learning. Kredit:Ozcan Lab, UCLA. Eksponering for partikler (PM) har været forbundet med
- Hvad ville der ske med Jorden og andre planeter i solsystemet uden Suns -gravitationskraft?
- Sådan finder du mønstre i Fractions
- Kæmpe magnetiske reb set i Whale Galaxys glorie
- Videnskab med funktioner menneskelig krop?
- Elektrisk 'Batmobile' afslører, hvordan kinesere har superbilmarkedet i kikkerten
- Hvorfor er DNA det svageste bevis for evolution?


