Hvor effektivt smelter saltis?
hvordan salt smelter is:
* frysningspunktdepression: Salt opløses i vand og sænker sit frysepunkt. En opløsning af salt og vand fryser ved en lavere temperatur end rent vand. Dette er grunden til, at salt kan smelte is, selvom temperaturen er under frysepunktet.
* smeltningsproces: Salt opløses i den tynde film af vand på isoverfladen og sænker frysningspunktet for dette vand. Dette gør det muligt for mere is at smelte, og processen fortsætter, når mere salt opløses.
Faktorer, der påvirker effektiviteten:
* salttype: Klippesalt (natriumchlorid) er det mest almindelige og omkostningseffektive, men andre salte som calciumchlorid og magnesiumchlorid er mere effektive ved lavere temperaturer.
* Koncentration: Højere koncentrationer af salt sænker frysepunktet mere effektivt, men overdreven salt kan være skadelig.
* Temperatur: Salt er mindre effektivt ved meget lave temperaturer. Nedenfor ca. -20 ° F (-29 ° C) vil salt ikke smelte is markant.
* istilstand: Kompakt, tæt is smelter langsommere end løs, fluffy sne.
* tilstedeværelse af urenheder: Snavs, sand og andre urenheder kan bremse smelteprocessen.
* applikationsmetode: Spredning af salt jævnt over isoverfladen sikrer maksimal effektivitet.
Effektivitetshensyn:
* Effektivitet: Salt er meget effektivt til smeltende is, men dens effektivitet falder ved lavere temperaturer.
* Miljøpåvirkning: Saltafstrømning kan forurene vandveje og skade vegetation. Brug af mindre salt eller alternative metoder er fordelagtigt for miljøet.
* Omkostninger: Rocksalt er den billigste mulighed, men andre salte er muligvis mere omkostningseffektivt på lang sigt på grund af deres større effektivitet.
Konklusion:
Salt er en meget anvendt og effektiv metode til smeltning af is, men dens effektivitet varierer afhængigt af forskellige faktorer. At forstå disse faktorer hjælper med at vælge den mest effektive og miljøvenlige tilgang til afisning.
 Varme artikler
Varme artikler
-
 Følger kemikaliernes vej gennem jordenForskere fra Aarhus Universitet har udviklet en forbedret metode til at følge transporten af kemikalier gennem jorden. Kredit:Janne Hansen Hvor bliver pesticider og deres nedbrydningsprodukter a
Følger kemikaliernes vej gennem jordenForskere fra Aarhus Universitet har udviklet en forbedret metode til at følge transporten af kemikalier gennem jorden. Kredit:Janne Hansen Hvor bliver pesticider og deres nedbrydningsprodukter a -
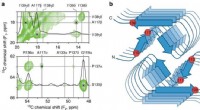 Forskere undersøger proteiner, der forårsager hjernesygdomme på atomniveauNøgleinterresidue kontakter og skematisk model af den humane PrP23-144 amyloid β-kerne. a Små områder af et 900 MHz todimensionalt 13C-13C DARR faststof-NMR-spektrum registreret med en blandingstid på
Forskere undersøger proteiner, der forårsager hjernesygdomme på atomniveauNøgleinterresidue kontakter og skematisk model af den humane PrP23-144 amyloid β-kerne. a Små områder af et 900 MHz todimensionalt 13C-13C DARR faststof-NMR-spektrum registreret med en blandingstid på -
 Stilladsmetoden gør det muligt for biokemikere at se proteiner i bemærkelsesværdige detaljerForskning fra UCLAs Tamir Gonen, venstre, Todd Yeates og Yuxi Liu, sammen med UCSFs Shane Gonen (ikke vist), giver værdifuld indsigt i komponenter i cellen. Kredit:Reed Hutchinson/UCLA UCLA-biokem
Stilladsmetoden gør det muligt for biokemikere at se proteiner i bemærkelsesværdige detaljerForskning fra UCLAs Tamir Gonen, venstre, Todd Yeates og Yuxi Liu, sammen med UCSFs Shane Gonen (ikke vist), giver værdifuld indsigt i komponenter i cellen. Kredit:Reed Hutchinson/UCLA UCLA-biokem -
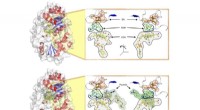 Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala
Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala
- Hvorfor ser vi Proxima Centauri på himlen?
- Hvad hedder videnskabelig undersøgelse af menneske og menneskeheden?
- Hvordan er en isotop af et atom, der er anderledes end ikke -isotop?
- COVID-19:Farerne ved en lige nok, just in time madsystem
- Hvad er betydningen af den nederste halvmåne i astrologi, og hvordan påvirker det vores daglige …
- Sjove fakta på havbunden


