Hvordan producerer du brintgas fra eddike?
Kemien:
* eddike er eddikesyre (CH3COOH). For at få brint (H2) skal du bryde de kemiske bindinger inden for eddikesyremolekylet.
* elektrolyse: Dette er den mest almindelige metode. Du bliver nødt til at bruge en stærk elektrisk strøm til at opdele vandmolekylerne (H2O) i eddike i brintgas (H2) og iltgas (O2).
* reaktion med et metal: Et stærkt metal som zink kan reagere med eddikesyre for at producere brintgas. Dette er en mere farlig metode på grund af produktionen af brandfarligt brint og reaktionens ætsende karakter.
Hvorfor er det ikke praktisk eller sikkert:
* Lavt udbytte: Eddike har en lav koncentration af eddikesyre, så mængden af produceret brint vil være lille.
* Sikkerhedsfarer: Elektrolyse kræver en betydelig elektrisk strøm, hvilket kan være farligt. Reaktioner med metaller kan være eksplosive, hvis ikke omhyggeligt kontrolleres.
* Potentiale for urenheder: Det producerede brint kan indeholde urenheder som ilt eller andre gasser, hvilket gør det uegnet til mange anvendelser.
Alternativer:
Hvis du er interesseret i at producere brint, er der mere sikre og mere effektive metoder:
* Elektrolyse af vand: Brug af en dedikeret elektrolyseopsætning med rent vand er en sikrere og mere effektiv måde at producere brint på.
* dampreformering af metan: Dette er en almindelig industriel proces, der producerer brint fra naturgas.
Det er vigtigt at huske, at det at arbejde med kemikalier og elektricitet kan være farligt. Hvis du er interesseret i brintproduktion, skal du kontakte pålidelige ressourcer og sikre dig, at du har det rette sikkerhedsudstyr og viden, før du forsøger nogen eksperimenter.
 Varme artikler
Varme artikler
-
 Forbindelser, der giver kaffen sin karakteristiske mundfølelseKredit:Pixabay/CC0 Public Domain Kaffedrikke genkender intuitivt fornøjelsen ved at sluge en glat, rig bryg versus en vandig. Bortset fra tilsat fløde eller sukker, selve kaffen bidrager til denne
Forbindelser, der giver kaffen sin karakteristiske mundfølelseKredit:Pixabay/CC0 Public Domain Kaffedrikke genkender intuitivt fornøjelsen ved at sluge en glat, rig bryg versus en vandig. Bortset fra tilsat fløde eller sukker, selve kaffen bidrager til denne -
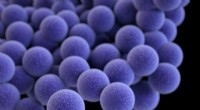 Forskere opdager gener, der hjælper skadelige bakterier til at modarbejde behandlingMethicillinresistent Staphylococcus aureus (MRSA). Kredit:Amerikanske centre for sygdomsbekæmpelse og forebyggelse Et Rutgers-ledet team har opdaget to gener, der gør nogle stammer af skadelige
Forskere opdager gener, der hjælper skadelige bakterier til at modarbejde behandlingMethicillinresistent Staphylococcus aureus (MRSA). Kredit:Amerikanske centre for sygdomsbekæmpelse og forebyggelse Et Rutgers-ledet team har opdaget to gener, der gør nogle stammer af skadelige -
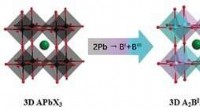 Forskere udvikler halogenid dobbelt perovskit ferroelektrikSkematisk illustration af metal-hetero-substitution og kationinterkalation fra 3-D blyhalogenidperovskiter til 2-D dobbelthalogenidperovskiter. Kredit:Prof. LUOs gruppe Halogenid -perovskitter har
Forskere udvikler halogenid dobbelt perovskit ferroelektrikSkematisk illustration af metal-hetero-substitution og kationinterkalation fra 3-D blyhalogenidperovskiter til 2-D dobbelthalogenidperovskiter. Kredit:Prof. LUOs gruppe Halogenid -perovskitter har -
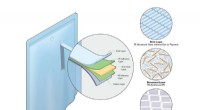 Bygger en bedre polyethylenEmballage, såsom juiceposer, er fremstillet med sammenbundne lag af metal, såsom aluminium, og forskellige typer plast, hvilket gør dem næsten umulige at genbruge. Fordi kun 1-3 procent af sådan embal
Bygger en bedre polyethylenEmballage, såsom juiceposer, er fremstillet med sammenbundne lag af metal, såsom aluminium, og forskellige typer plast, hvilket gør dem næsten umulige at genbruge. Fordi kun 1-3 procent af sådan embal
- Hvorfor har Pentanal et højere kogepunkt end 3-methylbutanal?
- Ligger 5 plus altid 10?
- Forskere afslører molekylær mekanisme for metamfetaminbinding til sporaminreceptor
- Hvor hurtigt kan en 11-årig løbe i mph?
- Beskriv ændringen i reaktionshastigheden, når enzymkoncentrationen øges?
- Nanopartikel-dekorerede celler driver en ny tilgang til kræftbehandling


