Hvad er reaktionen mellem metan og bromvand?
Her er en sammenbrud:
* bromvand er en rødbrun opløsning, der indeholder opløst brom (BR₂).
* methan er en farveløs og lugtfri gas.
reaktionen:
Reaktionen kræver UV -lys eller varme at fortsætte. I nærvær af lys eller varme bryder brommolekylet ned i bromradikaler (BR •), som er meget reaktive. Disse bromradikaler kan derefter angribe metanmolekylet og erstatte et hydrogenatom med et bromatom. Dette resulterer i dannelsen af bromethan (CH₃BR) og hydrogenbromid (HBR) .
Reaktionsligningen:
`` `
CH₄ + BR₂ → CH₃BR + HBR
`` `
Observationer:
* Den rødbrune farve på bromvandet vil fade Når brom reagerer med metan.
* hydrogenbromid (HBR) , en farveløs gas, vil blive produceret.
Bemærk:
Denne reaktion er en langsom proces og kan være ganske rodet . Det kræver omhyggelig kontrol af reaktionsbetingelserne for at forhindre dannelse af flere bromerede produkter.
Vigtigt:
Denne reaktion er et eksempel på en fri radikal reaktion . Frie radikaler er meget reaktive arter, der kan indlede kædereaktioner.
Sidste artikelEn anion af klor eller anden halogen?
Næste artikelHvor mange atomer i NAC2H3O2?
 Varme artikler
Varme artikler
-
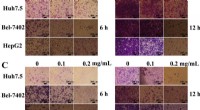 Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand
Marine bakterielt exopolysaccharid EPS11 hæmmer migration og invasion af levercancercellerFigur 1EPS11 hæmmer migration, invasion og kolonidannelse af levercancerceller (Huh7.5, Bel-7402, og HepG2 -cellelinjer). (A) Observation af fi liform-strukturer i Bel-7402 og HepG2-celler efter behand -
 Litauere udvikler en takeaway-madpakke, der er fuldstændig plastikfriKaunas borgere, forskere og virksomheder skabte en innovativ madpakke med madpakke under en fælles workshop. Kredit:KTU Takeaway mad er blevet en integreret del af vores liv. På trods af bekvemmeli
Litauere udvikler en takeaway-madpakke, der er fuldstændig plastikfriKaunas borgere, forskere og virksomheder skabte en innovativ madpakke med madpakke under en fælles workshop. Kredit:KTU Takeaway mad er blevet en integreret del af vores liv. På trods af bekvemmeli -
 Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ
Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ -
 Forskere skaber en kemisk rumkortlægningsmetode og knækker mysteriet om Mendeleev-nummeretKort over sammensat hårdhed. Kredit:Artem R. Oganov Forskere har længe søgt efter et system til at forudsige materialers egenskaber baseret på deres kemiske sammensætning. I særdeleshed, de sætter
Forskere skaber en kemisk rumkortlægningsmetode og knækker mysteriet om Mendeleev-nummeretKort over sammensat hårdhed. Kredit:Artem R. Oganov Forskere har længe søgt efter et system til at forudsige materialers egenskaber baseret på deres kemiske sammensætning. I særdeleshed, de sætter
- Sådan laver du et ægflugt ved hjælp af salt til en videnskabsprojekt
- Den amerikanske teknologisektor oplever kun beskeden lettelse i Kinas handelsaftale
- Hvad klassificerede Linnaeus organismer ud fra deres ligheder?
- Hvilken energi overføres ved direkte kontakt eller berøring?
- Hvordan fremstilles jern i stål?
- NASA-NOAA-satellitten fanger orkanen Nana, der går i land i ly af natten


