Hvorfor er gas en god isolator?
* lav densitet: Gasmolekyler er meget spredt sammenlignet med væsker og faste stoffer. Dette betyder, at der er færre muligheder for kollisioner og energioverførsel mellem molekylerne.
* svage intermolekylære kræfter: De kræfter, der holder gasmolekyler sammen, er meget svage. Dette betyder, at de ikke let deler eller overfører energi, hvilket er et centralt krav til varmeoverførsel.
* fri bevægelighed: Gasmolekyler bevæger sig frit og tilfældigt, hvilket gør det vanskeligt for dem at danne en kontinuerlig sti til varmeledning.
Dette betyder dog ikke, at alle gasser er perfekte isolatorer:
* konvektion: Selvom gasser er dårlige ledere, kan de overføre varme gennem konvektion. Det er her varme overføres af bevægelsen af selve gassen. For eksempel skaber varm luft stigende og køligere luft synkende konvektionsstrømme.
* Polaritet: Gasser som vanddamp (H2O) er polære molekyler. Dette betyder, at de har en positiv og negativ ende, så de kan interagere stærkere med hinanden og potentielt udføre varme bedre.
Eksempler på gasser, der bruges som isolatorer:
* luft: Den mest almindelige isolator. Vi bruger det til at fylde vægge, vinduer og andre rum for at forhindre varmeoverførsel.
* nitrogen: En inert gas, der ofte bruges til isolering, fordi den er meget stabil og ikke reagerer let.
* Argon: En anden inert gas, der bruges til isolering. Det har bedre isolerende egenskaber end nitrogen ved højere temperaturer.
Kortfattet: Gasser er generelt gode isolatorer på grund af deres lave densitet, svage intermolekylære kræfter og frie bevægelse af molekyler. Nogle gasser kan dog være bedre isolatorer end andre, og konvektion kan stadig spille en rolle i varmeoverførsel.
Sidste artikelHvad er vismuthchlorid i?
Næste artikelLigninger til reaktionerne af kaliumhydroxid og nitrogen Poostink?
 Varme artikler
Varme artikler
-
 Forskere forvandler ikke-giftige rester til belægning, der modstår slid, plet og sollysEn stol påført lignin. Kredit:Fotoni Film &Communications På grund af den globale indsats for at opfylde bæredygtighedsstandarder, mange lande søger i øjeblikket at erstatte beton med træ i bygnin
Forskere forvandler ikke-giftige rester til belægning, der modstår slid, plet og sollysEn stol påført lignin. Kredit:Fotoni Film &Communications På grund af den globale indsats for at opfylde bæredygtighedsstandarder, mange lande søger i øjeblikket at erstatte beton med træ i bygnin -
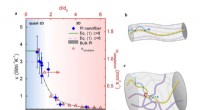 Tilfældig gang mellem varmebærere i amorfe polymerer(a) Diameterafhængigheden af termisk ledningsevne af polyimid -nanofibre. Romben repræsenterer eksperimentdata. Der er en dimensionel crossover af varmediffusion i molekylære kæder fra quasi-1D til
Tilfældig gang mellem varmebærere i amorfe polymerer(a) Diameterafhængigheden af termisk ledningsevne af polyimid -nanofibre. Romben repræsenterer eksperimentdata. Der er en dimensionel crossover af varmediffusion i molekylære kæder fra quasi-1D til -
 Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske
Ny metode til at bekæmpe kræft med molekylære fibreKræftcellernes fysiske strukturer forstyrres af en bane, der danner indersiden af cellerne - hvilket aktiverer deres selvdestruktionsmekanisme. Kredit:MPI-P Ifølge Tysklands forbundsstatistiske -
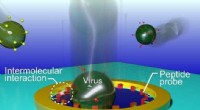 Ny viral identifikationsmetode udvikletFig. Enkeltvirus-detektioner ved ioniske strømmålinger i en peptid-dekoreret Au nanopore. Kredit:Osaka University I øjeblikket, influenzatypning i klinisk praksis udføres ved anvendelse af en immu
Ny viral identifikationsmetode udvikletFig. Enkeltvirus-detektioner ved ioniske strømmålinger i en peptid-dekoreret Au nanopore. Kredit:Osaka University I øjeblikket, influenzatypning i klinisk praksis udføres ved anvendelse af en immu
- NASA ser Tropical Cyclone 5 dannes nær den nordvestlige australske kyst
- Forskere identificerer vanskeligheder med at balancere terrorisme mediedækning
- Hvilken rigelig gas fra atmosfæren viser største variation fra sted til overflade?
- Hvad er chancerne? Sandsynlighed løser et evolutionært puslespil
- Privatiserede fængsler fører til flere indsatte, længere sætninger, undersøgelse finder
- Hvilken effekt havde den tro, som de fleste var med, blandinger på kemi?


