Hvad er nitrogener molekylær form?
Her er hvorfor:
* nitrogens elektroniske konfiguration: Nitrogen har fem valenselektroner. I N₂ danner det en tredobbelt binding med et andet nitrogenatom, der deler tre elektronpar.
* VSEPR -teori: I henhold til Valence Shell Electron Pair Repulsion (VSEPR) teori, parrer elektron omkring et centralt atomatom hinanden og prøver at forblive så langt fra hinanden som muligt.
* lineær form: I N₂ er de to nitrogenatomer og de tre delte elektronpar (tredobbelt binding) alle i en lige linje, hvilket minimerer frastødelse.
Derfor har nitrogengas (N₂) en lineær molekylær form.
Sidste artikelHvad er C2H4 den molekylære formel til?
Næste artikelHvad er den molekylære formel for ethylenglycol, hvis masse 62 amu?
 Varme artikler
Varme artikler
-
 Affaldsplast, der omdannes til filtreringsmembranerBruno Pulido tester effektiviteten af holdets syntetiske membran. Kredit:KAUST I en verden, der synes at drukne i plastflasker, genanvendelse af dette affald til nyttige materialer ville bidrage
Affaldsplast, der omdannes til filtreringsmembranerBruno Pulido tester effektiviteten af holdets syntetiske membran. Kredit:KAUST I en verden, der synes at drukne i plastflasker, genanvendelse af dette affald til nyttige materialer ville bidrage -
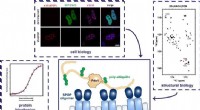 Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr
Hvordan ved et reguleringsprotein, hvor det skal bindes for at modulere insulinproduktionen?Penn State -forskere brugte en række forskellige teknikker vedrørende cellebiologi, strukturel biologi, og proteinbiofysik for at bestemme, hvordan proteinerne SPOP og Pdx1 fungerer sammen for at sikr -
 At tænke uden for buret:En ny tilgang til energiintensive molekylære adskillelserKAUST-forskere udvikler organiske burlignende materialer til at adskille xylenisomerer på en mere energieffektiv måde. Kredit:KAUST; Anastasia Serin En omvendt form for vært-gæstekemi kunne hæmme
At tænke uden for buret:En ny tilgang til energiintensive molekylære adskillelserKAUST-forskere udvikler organiske burlignende materialer til at adskille xylenisomerer på en mere energieffektiv måde. Kredit:KAUST; Anastasia Serin En omvendt form for vært-gæstekemi kunne hæmme -
 Flydende svovl ændrer form og bliver kritisk under trykMohamed Mezouar, tilsvarende forfatter og ESRF -videnskabsmand, under forsøget på ESRF, den europæiske synkrotron. Kredit:ESRF/Stef Candé Forskere fra ESRF, sammen med teams fra CEA og CNRS/Sorbon
Flydende svovl ændrer form og bliver kritisk under trykMohamed Mezouar, tilsvarende forfatter og ESRF -videnskabsmand, under forsøget på ESRF, den europæiske synkrotron. Kredit:ESRF/Stef Candé Forskere fra ESRF, sammen med teams fra CEA og CNRS/Sorbon
- Antarktis skjulte landskab formet af floder i varmere æra
- Ny teknologi, der bruger sølv, kan være nøglen til elektroniske fremskridt
- Hvad kaldes det, når et stof, der blev dannet under reaktion, der blev fundet på højre side af pi…
- Med 30, 000 undersøgelser, forskere bygger go-to datasættet for småbrugsbedrifter
- Hvordan virker håndvarmere? Et videnskabeligt blik
- Undersøgelse undersøger årsagerne til jordskælv, der stammer dybt under jordens overflade


