En beholder med ilt ved 22 grader Celsius og 740 mm Hg afkøles til -22 Hvad det nye trykgas?
forståelse af koncepterne
* Kombineret gaslov: Denne lov relaterer tryk, volumen og temperatur på en gas. Det siger:(p₁v₁)/t₁ =(p₂v₂)/t₂
* tryk og temperaturforhold: For en fast mængde gas er tryk direkte proportional med absolut temperatur. Dette betyder, at hvis du reducerer temperaturen, vil trykket også falde.
Løsning af problemet
1. Konverter temperaturer til Kelvin:
* T₁ =22 ° C + 273,15 =295,15 K
* T₂ =-22 ° C + 273,15 =251,15 K
2. Antag konstant volumen: Da problemet ikke nævner en ændring i volumen, antager vi, at volumen (V) forbliver konstant. Dette betyder V₁ =V₂.
3. Anvend den kombinerede gaslov:
* (P₁v₁)/t₁ =(p₂v₂)/t₂
* Da v₁ =V₂, kan vi annullere dem:P₁/T₁ =P₂/T₂
4. Løs for P₂ (det nye pres):
* P₂ =(p₁ * t₂) / t₁
* P₂ =(740 mmHg * 251,15 K) / 295,15 K
* P₂ ≈ 630 mmHg
Derfor er det nye tryk på iltgassen ca. 630 mmHg.
Sidste artikelHvad er det kemiske navn på LIO?
Næste artikelEr bestemt kemisk sammensætning et kendetegn ved mineraler?
 Varme artikler
Varme artikler
-
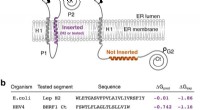 Forskning viser rollen af intra-mebrane interaktioner i viral kontrol af celledødFig. 1:Insertion af vBcl2 Ct hydrofobe sekvenser i eukaryote membraner. Fra:Viralt Bcl2s ’transmembrane domæne interagerer med vært Bcl2 proteiner for at kontrollere cellulær apoptose En forskergr
Forskning viser rollen af intra-mebrane interaktioner i viral kontrol af celledødFig. 1:Insertion af vBcl2 Ct hydrofobe sekvenser i eukaryote membraner. Fra:Viralt Bcl2s ’transmembrane domæne interagerer med vært Bcl2 proteiner for at kontrollere cellulær apoptose En forskergr -
 Nye test identificerer forurenet drikkevand på få minutter, ikke ugerLegionellaceller kan påvises med en testmaskine i hjemmeprinterstørrelse. Kredit:CDC/ Dr. Barry S. Fields Hurtig, overkommelige vandtest, der kan bruges på stedet og endda køre kontinuerligt, vil
Nye test identificerer forurenet drikkevand på få minutter, ikke ugerLegionellaceller kan påvises med en testmaskine i hjemmeprinterstørrelse. Kredit:CDC/ Dr. Barry S. Fields Hurtig, overkommelige vandtest, der kan bruges på stedet og endda køre kontinuerligt, vil -
 Opskalering af tannin-varmtvandsudvindingKredit:BBEPP Rehap kortlagde for nylig den rigelige forsyning af skovbrugsaffald i Europa, og hvor det mest bæredygtigt kan hentes fra. Med denne viden, Projektstudier har forsket i den bedst egne
Opskalering af tannin-varmtvandsudvindingKredit:BBEPP Rehap kortlagde for nylig den rigelige forsyning af skovbrugsaffald i Europa, og hvor det mest bæredygtigt kan hentes fra. Med denne viden, Projektstudier har forsket i den bedst egne -
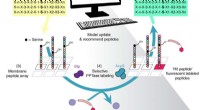 Brug af maskinlæring til at designe peptiderOversigt over den iterative Peptid Optimering med Optimal Learning (POOL) metode workflow. Kredit: Naturkommunikation (2018). DOI:10.1038/s41467-018-07717-6 Forskere og ingeniører har længe været
Brug af maskinlæring til at designe peptiderOversigt over den iterative Peptid Optimering med Optimal Learning (POOL) metode workflow. Kredit: Naturkommunikation (2018). DOI:10.1038/s41467-018-07717-6 Forskere og ingeniører har længe været
- Hvad hedder energien forbundet med smeltning?
- Undersøgelse viser, at mikrofinansiering kan hjælpe, også selvom målene ikke er nået
- Forskere udvikler en ny metode til at detektere kernedannelse
- Hvor mange atomer i C2H5NO2?
- Hvilken del af afbalanceret kemisk ligning giver information om de relative tal mol -reaktanter og p…
- Undersøgelse sammenligner Fox News og MSNBC ved hjælp af 52, 000 udskrifter, 283 millioner ord


