I raffinering af sølvgenvinding fra nitratopløsning involveret forskydning af kobbermetalskrivningsreaktion involveret?
2agno₃ (aq) + cu (s) → cu (no₃) ₂ (aq) + 2ag (s)
Forklaring:
* agno₃ (aq) Repræsenterer sølvnitrat opløst i vand (vandig opløsning).
* cu (s) Repræsenterer fast kobbermetal.
* cu (no₃) ₂ (aq) Repræsenterer kobber (II) nitrat opløst i vand.
* 2ag (r) Repræsenterer fast sølvmetal.
hvordan det fungerer:
1. forskydning: Jo mere reaktivt kobbermetal fortrænger de mindre reaktive sølvioner (AG⁺) fra sølvnitratopløsningen.
2. redoxreaktion: Dette er en redoxreaktion, hvor kobber oxideres (mister elektroner) og sølv reduceres (får elektroner).
3. Dannelse af kobbernitrat: Kobberionerne (Cu²⁺) dannet derefter kombineres med nitrationerne (NO₃⁻) for at skabe kobber (II) nitrat.
4. fast sølv: De fordrevne sølvioner får elektroner og bliver solid sølvmetal, som kan opsamles og raffineres yderligere.
Nøglepunkter:
* Kobber er et bedre reduktionsmiddel end sølv.
* Reaktionen er eksoterm, hvilket betyder, at den frigiver varme.
* Denne metode er en relativt enkel og omkostningseffektiv måde at udtrække sølv fra opløsninger på.
Sidste artikelHvad er det videnskabelige navn for væske til solid?
Næste artikelHvorfor er kogepunktet for NaCl højere end saccharose?
 Varme artikler
Varme artikler
-
 Ny chip måler flere cellulære reaktioner for at fremskynde opdagelse af lægemidlerCMOS multimodal cellulær interface array chip i drift i et standard biologilaboratorium. Kredit:Georgia Institute of Technology At finde måder at forbedre lægemiddeludviklingsprocessen – som i øje
Ny chip måler flere cellulære reaktioner for at fremskynde opdagelse af lægemidlerCMOS multimodal cellulær interface array chip i drift i et standard biologilaboratorium. Kredit:Georgia Institute of Technology At finde måder at forbedre lægemiddeludviklingsprocessen – som i øje -
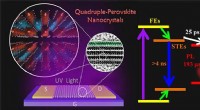 Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk
Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk -
 Enkel metode til keramisk-baserede fleksible elektrolytplader til lithiummetalbatterierI den nærmeste fremtid, lithiummetalbatterier med en fleksibel LLZO elektrolytplade kan bruges i avancerede elektriske køretøjer (EVer). Kredit:Tokyo Metropolitan University 1000°C) processer. Den
Enkel metode til keramisk-baserede fleksible elektrolytplader til lithiummetalbatterierI den nærmeste fremtid, lithiummetalbatterier med en fleksibel LLZO elektrolytplade kan bruges i avancerede elektriske køretøjer (EVer). Kredit:Tokyo Metropolitan University 1000°C) processer. Den -
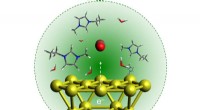 Kunstig fotosyntese omdanner kuldioxid til flydende brændstofferUnder grønt lys og assisteret af en ionisk væske, guld nanopartikler, bund, låne elektroner til at omdanne CO2-molekyler, de røde og grå kugler i midten, til mere komplekse kulbrintebrændstofmolekyler
Kunstig fotosyntese omdanner kuldioxid til flydende brændstofferUnder grønt lys og assisteret af en ionisk væske, guld nanopartikler, bund, låne elektroner til at omdanne CO2-molekyler, de røde og grå kugler i midten, til mere komplekse kulbrintebrændstofmolekyler


