Hvad er nogle kovalente forbindelser af magnesium?
* magnesiumchlorid (MGCL₂): Dette er faktisk en ionisk forbindelse, men den kan eksistere i en kovalent form i gasfasen.
* magnesiumoxid (MGO): Dette er også typisk ionisk, men udviser en vis kovalent karakter på grund af den høje elektronegativitetsforskel mellem magnesium og ilt.
* magnesiumnitrid (mg₃n₂): Denne forbindelse er ionisk, men har en vis kovalent karakter.
* magnesiumhydrid (MGH₂): Denne forbindelse er for det meste ionisk, men har en vis kovalent karakter, hvilket gør det til et nyttigt brintopbevaringsmateriale.
kovalente forbindelser af magnesium med ikke -metaller:
* magnesiumbromid (MGBR₂): En kovalent forbindelse i gasfasen.
* magnesiumiodid (mgi₂): En kovalent forbindelse i gasfasen.
* magnesiumsulfid (MGS): En kovalent forbindelse i gasfasen, men den udviser en vis ionisk karakter i fast tilstand.
* magnesium selenid (MGSE): En kovalent forbindelse i gasfasen.
* Magnesium Telluride (MGTE): En kovalent forbindelse i gasfasen.
Det er vigtigt at bemærke, at den kovalente karakter af disse forbindelser generelt er svag. Magnesium er et meget elektropositivt element, og dets elektronegativitetsforskel med de fleste ikke -metaller er betydelig, hvilket fører til primært ionisk binding.
Under visse betingelser, som i gasfasen eller i visse kemiske reaktioner, kan de kovalente karakter af disse forbindelser imidlertid blive mere fremtrædende.
 Varme artikler
Varme artikler
-
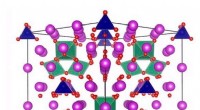 Finjustering af kemi ved doping med overgangsmetaller gav stabilitet i bismuthoxidKredit:Australian Nuclear Science and Technology Organisation (ANSTO) ANSTO har bidraget til forskning ledet af University of Sydney, involverer doping af overgangsmetaller i en polymorf af bismut
Finjustering af kemi ved doping med overgangsmetaller gav stabilitet i bismuthoxidKredit:Australian Nuclear Science and Technology Organisation (ANSTO) ANSTO har bidraget til forskning ledet af University of Sydney, involverer doping af overgangsmetaller i en polymorf af bismut -
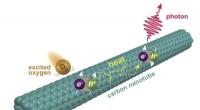 Kemikere får et kig på ny fluorescens i kulstofnanorørKemikere ved Rice University har opdaget et andet niveau af fluorescens i enkeltvæggede kulstofnanorør. Fluorescensen udløses, når oxygenmolekyler exciteret til en singlettilstand interagerer med nano
Kemikere får et kig på ny fluorescens i kulstofnanorørKemikere ved Rice University har opdaget et andet niveau af fluorescens i enkeltvæggede kulstofnanorør. Fluorescensen udløses, når oxygenmolekyler exciteret til en singlettilstand interagerer med nano -
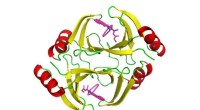 Undersøgelse giver nye spor til forbedring af kemoterapierStrukturen af proteinet kodet af tnmS3-genet. Kredit:Shen Lab/Scripps Research Omkring halvdelen af alle stoffer, lige fra morfin til penicillin, kommer fra forbindelser, der er fra - eller er
Undersøgelse giver nye spor til forbedring af kemoterapierStrukturen af proteinet kodet af tnmS3-genet. Kredit:Shen Lab/Scripps Research Omkring halvdelen af alle stoffer, lige fra morfin til penicillin, kommer fra forbindelser, der er fra - eller er -
 Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ
Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ
- Hvordan påvirker de naturlige ressourcer i en region, hvilke produkter folk fremstiller?
- Afsky driver nogle religiøse tanker og følelser - ny forskning tyder på
- Hvorfor buffer modstå ændringer i PH, når en lille mængde syre eller base tilsættes?
- Hvordan formede kontinentale isplader landskabet i det nordvestlige højland?
- Hvad hedder tektonisk plade, der inkluderer os?
- Kosmiske kannibaler driver jetfly ud i rummet med 40 % lyshastighed


