Hvorfor er klor mere reaktiv end argon?
Her er en sammenbrud:
* klor (Cl): Har 17 elektroner med en elektronkonfiguration på 2, 8, 7. Det har kun brug for endnu en elektron for at afslutte sin yderste skal og opnå en stabil oktet som de ædle gasser. Dette gør det meget reaktivt og let at vinde et elektron gennem kemiske reaktioner.
* argon (AR): Har 18 elektroner med en komplet yderste skal (2, 8, 8). Denne stabile konfiguration gør den meget ureaktiv, da den ikke let vinder eller mister elektroner.
Kortfattet:
* Chlor er reaktiv Fordi det ønsker at få et elektron for at opnå en stabil oktet.
* Argon er ureaktiv Fordi det allerede har en stabil oktet.
Denne forskel i reaktivitet er et centralt kendetegn ved elementer og deres placering på den periodiske tabel. Elementer på højre side af bordet (halogener som klor) har en tendens til at være meget reaktive på grund af deres behov for yderligere elektroner, mens ædle gasser langt til højre er meget ureaktive på grund af deres fulde ydre skaller.
 Varme artikler
Varme artikler
-
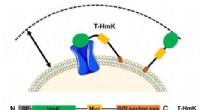 Zombie-scanning muliggør undersøgelse af peptid-receptor-interaktioner på celleoverfladenDet bundne toksin (T-HmK) trækkes fri og bindes til en kaliumkanal (blå) udtrykt i cellemembranen. Reaktionsvolumenet, som en T-HmK kan besøge (pil med to hoveder) bestemmes af de kombinerede længder
Zombie-scanning muliggør undersøgelse af peptid-receptor-interaktioner på celleoverfladenDet bundne toksin (T-HmK) trækkes fri og bindes til en kaliumkanal (blå) udtrykt i cellemembranen. Reaktionsvolumenet, som en T-HmK kan besøge (pil med to hoveder) bestemmes af de kombinerede længder -
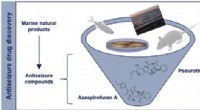 Svamp i Rødehavet giver spor til nye epilepsimedicinKredit:American Chemical Society Nye behandlinger for epilepsi er hårdt nødvendige, fordi den nuværende medicin ikke virker for mange mennesker med sygdommen. For at finde nye kundeemner, forskere
Svamp i Rødehavet giver spor til nye epilepsimedicinKredit:American Chemical Society Nye behandlinger for epilepsi er hårdt nødvendige, fordi den nuværende medicin ikke virker for mange mennesker med sygdommen. For at finde nye kundeemner, forskere -
 Den kommende forstyrrelse af OLED-teknologierEn organisk lysemitterende diode (OLED) er en selvlysende, tyndfilmskomponent lavet af organiske halvledende materialer. Da der ikke er behov for siliciumchips, kun pigmentmolekyler disse lys kan prod
Den kommende forstyrrelse af OLED-teknologierEn organisk lysemitterende diode (OLED) er en selvlysende, tyndfilmskomponent lavet af organiske halvledende materialer. Da der ikke er behov for siliciumchips, kun pigmentmolekyler disse lys kan prod -
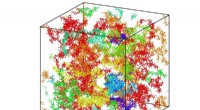 Ny teori styrker det, vi ved om, hvordan ladede makromolekyler samler sig selvKredit:Shibananda Das I en opdagelse med vidtrækkende implikationer annoncerede forskere ved University of Massachusetts Amherst for nylig i Proceedings of the National Academy of Sciences at ensar
Ny teori styrker det, vi ved om, hvordan ladede makromolekyler samler sig selvKredit:Shibananda Das I en opdagelse med vidtrækkende implikationer annoncerede forskere ved University of Massachusetts Amherst for nylig i Proceedings of the National Academy of Sciences at ensar
- NASAs nyligt omdøbte Swift Mission udspionerer en kometafmatning
- Omprogrammerbar satellit brændt før opsendelse
- Hvad er den almindelige form for inputenergi. hvorfor?
- Opdagelse af biomateriale muliggør 3D-udskrivning af vævslignende vaskulære strukturer
- Undersøgelse af tågen IRAS 00500+6713 tyder på, at dens centrale stjerne er ulig nogen set før
- Hvordan man beregner osmolaritet i betragtning Liters


