Er manganacetatopløselig i vand?
Her er hvorfor:
* ionisk forbindelse: Manganacetat (Mn (ch₃coo) ₂) er en ionisk forbindelse. Ioniske forbindelser opløses generelt godt i vand, fordi vandmolekylerne kan omringe og trække de positivt og negativt ladede ioner fra hinanden.
* Polaritet: Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv og negativ ende. Den positive ende af vandmolekyler tiltrækker de negativt ladede acetationer (ch₃coo⁻), mens den negative ende tiltrækker de positivt ladede manganioner (MN²⁺). Denne interaktion hjælper med at bryde de ioniske bindinger fra hinanden og opløse forbindelsen.
Bemærk: Mens manganacetat generelt er opløselig i vand, kan opløseligheden påvirkes af faktorer som temperatur og tilstedeværelsen af andre opløste stoffer.
 Varme artikler
Varme artikler
-
 Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder
Redesigner håndsprit og donerer 7, 000 gallons til at bekæmpe COVID-19Håndsprit reddet af ethanol. Et velgørende initiativ kørte for at forhindre håndsprit i at løbe kritisk lavt over hele landet. Kredit:Georgia Tech/Christopher Moore Så mange mennesker, Seth Marder -
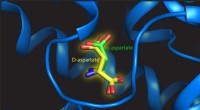 Montering af en højre hånd i en venstrehåndsvanteDenne illustration viser L- og D-aspartat på bindingsstedet for transportproteinet. Kredit:Valentina Arkhipova, University of Groningen Mange biomolekyler findes i to versioner, der er hinandens s
Montering af en højre hånd i en venstrehåndsvanteDenne illustration viser L- og D-aspartat på bindingsstedet for transportproteinet. Kredit:Valentina Arkhipova, University of Groningen Mange biomolekyler findes i to versioner, der er hinandens s -
 Lab udvikler dual-overflade grafenelektrode til at splitte vand i hydrogen og iltEn tosidet elektrokatalysator udviklet ved Rice University deler vand i hydrogen på den ene side og ilt på den anden. Hydrogensiden, der ses i elektronmikroskopbilleder, har platinpartikler (de mørke
Lab udvikler dual-overflade grafenelektrode til at splitte vand i hydrogen og iltEn tosidet elektrokatalysator udviklet ved Rice University deler vand i hydrogen på den ene side og ilt på den anden. Hydrogensiden, der ses i elektronmikroskopbilleder, har platinpartikler (de mørke -
 Håndholdt gadget til hurtig test af fødevarekvalitetKredit:El Nariz, Shutterstock En mikrobiologisk detektionsanordning vil hjælpe med at fremskynde målingen af forurening i råt kød, dermed minimere omkostninger og madspild. Fødevarebårne sygdom
Håndholdt gadget til hurtig test af fødevarekvalitetKredit:El Nariz, Shutterstock En mikrobiologisk detektionsanordning vil hjælpe med at fremskynde målingen af forurening i råt kød, dermed minimere omkostninger og madspild. Fødevarebårne sygdom
- Incivility på arbejdet:bliver dronninge-bi-syndromet værre?
- Tips til at leve online:Lektioner fra seks måneder af COVID-19-pandemien
- Forskere og filosof går sammen, foreslå en ny måde at kategorisere mineraler på
- Luftforurening falder i Indien efter lockdown
- Hvad er koloniens morfologi for Pseudomonas fluorescens?
- Fysiske egenskaber ved Styrofoam


