Natrium- og chloridatomer kombineres let, fordi de begge har en tendens til at miste elektroner?
* natrium (NA) har en enkelt elektron i sin yderste skal. Det mister let Denne elektron for at opnå en stabil elektronkonfiguration som neon.
* klor (Cl) Har syv elektroner i sin yderste skal. Det er let vinder En elektron for at opnå en stabil elektronkonfiguration som Argon.
Årsagen til, at natrium og klor kombineres let skyldes deres modsatte tendenser:
* Natrium ønsker at miste et elektron (for at blive positivt ladet)
* Chlor ønsker at få et elektron (for at blive negativt ladet)
Denne forskel i elektronegativitet (tendensen til at tiltrække elektroner) skaber en elektrostatisk attraktion mellem natrium- og chloridioner, der danner den ioniske forbindelse natriumchlorid (NaCl) eller bordsalt.
 Varme artikler
Varme artikler
-
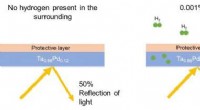 Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af
Forskere udvikler en alsidig brintsensorFigur 1. Skematisk illustration af, hvordan optiske brintsensorer fungerer. I nærheden af brint, det tantal- (Ta) og palladium- (Pd)-baserede materiale absorberer hydrogen (H). Jo større mængden af -
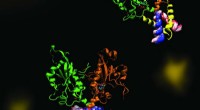 En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion
En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion -
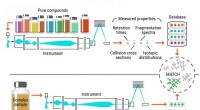 Ny tilgang til metabolomics-forskning kan vise sig at ændre spilletIllustration af den konventionelle identifikationsproces af metabolitter. Kredit:Pacific Northwest National Laboratory Nøjagtig identifikation af metabolitter, og andre små kemikalier, i biologisk
Ny tilgang til metabolomics-forskning kan vise sig at ændre spilletIllustration af den konventionelle identifikationsproces af metabolitter. Kredit:Pacific Northwest National Laboratory Nøjagtig identifikation af metabolitter, og andre små kemikalier, i biologisk -
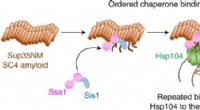 Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI
Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI
- Får vi en trist poop -emoji? Nå, der er en proces
- Nanostrukturer, der bruges som biosensorer, gør det muligt at påvise sygdomme eller allergener
- NASA-NOAA satellitsporing af den tropiske cyklon Kenanga
- ShotSpotter forbedrer detektion og respons på skud, men reducerer ikke kriminalitet, viser forsknin…
- Forskere skaber de første superspejle i mellem-infrarødt område
- Hawaii foreslår forbud mod visse solcremer for at redde koralrev


