Hvilke forbindelser dannes, når en syre reagerer med oxid?
1. Metaloxider:
* Grundlæggende oxider: Disse oxider reagerer med syrer for at danne salt og vand. Dette er en klassisk neutraliseringsreaktion.
Eksempel:
* Natriumoxid (Na₂o) + saltsyre (HCI) → natriumchlorid (NaCl) + vand (H₂O)
* amfoteriske oxider: Disse oxider kan reagere med både syrer og baser. Når de reagerer med syrer, danner de salt og vand .
Eksempel:
* Aluminiumoxid (al₂o₃) + svovlsyre (H₂so₄) → aluminiumssulfat (al₂ (SO₄) ₃) + vand (H₂O)
2. Ikke-metaloxider:
* Sure oxider: Disse oxider reagerer med syrer for at danne mere komplekse syrer .
Eksempel:
* Svovldioxid (SO₂) + vand (H₂O) → svovlsyre (H₂so₃)
Bemærk:
* Den specifikke salt, der er dannet, afhænger af den involverede specifikke syre- og metaloxid.
* Ikke alle metaloxider er basale, og ikke alle ikke-metaloxider er sure. Det er vigtigt at overveje oxidets specifikke kemiske egenskaber.
Kortfattet:
* Grundlæggende og amfoteriske metaloxider Reager med syrer for at danne salt og vand.
* sure ikke-metaloxider Reager med syrer for at danne mere komplekse syrer.
 Varme artikler
Varme artikler
-
 Nobelprisen for banebrydende måde at bygge molekyler på, der gjorde kemi grønnereList (til venstre) og MacMillan (til højre) er vindere af Nobelprisen i kemi i 2021. Kredit:NobelPrize.org, CC BY-SA Benjamin List og David MacMillan, fra henholdsvis Tyskland og USA, vil dele de
Nobelprisen for banebrydende måde at bygge molekyler på, der gjorde kemi grønnereList (til venstre) og MacMillan (til højre) er vindere af Nobelprisen i kemi i 2021. Kredit:NobelPrize.org, CC BY-SA Benjamin List og David MacMillan, fra henholdsvis Tyskland og USA, vil dele de -
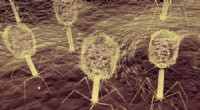 Viruss mangestrengede angreb på bakterier peger på nye måder at bekæmpe infektion påFager angriber en bakterie. Kredit:Imperial College London Forskere har afdækket, hvordan en virus anvender et todelt angreb mod et enkelt protein for at dræbe bakterier. Den internationale grupp
Viruss mangestrengede angreb på bakterier peger på nye måder at bekæmpe infektion påFager angriber en bakterie. Kredit:Imperial College London Forskere har afdækket, hvordan en virus anvender et todelt angreb mod et enkelt protein for at dræbe bakterier. Den internationale grupp -
 Forskere løser strukturen af intellektuelt handicap proteinKredit:University of Dundee Forskere ved University of Dundee har identificeret virkningerne af en mutation, der giver anledning til en form for intellektuel handicap. intellektuel funktionsnedsæ
Forskere løser strukturen af intellektuelt handicap proteinKredit:University of Dundee Forskere ved University of Dundee har identificeret virkningerne af en mutation, der giver anledning til en form for intellektuel handicap. intellektuel funktionsnedsæ -
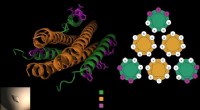 Forskere udvikler en bedre måde at blokere vira, der forårsager luftvejsinfektioner i barndommenDet antivirale peptid består af tre proptrækkere (i grønt), som låser sig omkring virussens fusionsprotein (i orange) for at forhindre virussen i at trænge ind i cellerne. Gellman-laboratoriet tilføje
Forskere udvikler en bedre måde at blokere vira, der forårsager luftvejsinfektioner i barndommenDet antivirale peptid består af tre proptrækkere (i grønt), som låser sig omkring virussens fusionsprotein (i orange) for at forhindre virussen i at trænge ind i cellerne. Gellman-laboratoriet tilføje
- Hvordan er spektret af hvidt lys fra solen?
- For at spare energi, AI rydder op i overskyede vejrudsigter
- Hvilke pH-numre betragtes som sure, basiske og neutrale?
- Cyklonen rammer Bangladesh, da næsten en million flygter ind i landet for at søge ly
- Hvilket mineral har en perle -glans og konchoidal brud?
- Hvad er de to reaktioner af aerob cellulær respiration?


