En 2,9990 g prøve af en ny forbindelse er blevet analyseret og fundet at indeholde følgende masserelementer Carbon 1.1610 brint 0.29240 Oxygen 1.5455 Beregn empirisk formel?
1. Konverter masse til mol
* carbon: (1.1610 g C) / (12.011 g / mol C) =0,09666 mol C
* brint: (0,29240 g h) / (1,008 g / mol h) =0,2900 mol h
* ilt: (1.5455 g o) / (15.9994 g / mol o) =0,09659 mol o
2. Find det enkleste molforhold
Del hver molværdi med den mindste molværdi (0,09659 mol o i dette tilfælde):
* carbon: 0,09666 mol C / 0,09659 mol o ≈ 1
* brint: 0,2900 mol H / 0,09659 mol o ≈ 3
* ilt: 0,09659 mol O / 0,09659 mol o ≈ 1
3. Skriv den empiriske formel
Den empiriske formel repræsenterer det enkleste forhold mellem hele antal atomer i forbindelsen. Baseret på molforholdene er den empiriske formel ch₃o .
Sidste artikelHvad er dannelsesvarmen SO2?
Næste artikelHvad er den ioniske ligning for hydrofluorinsyre og natriumhydroxid?
 Varme artikler
Varme artikler
-
 Ingeniører finder ud af, hvorfor nedfaldne blade på togskinner er så glatteKredit:Pixabay/CC0 Public Domain Et team af ingeniører ved University of Sheffield har fundet en forklaring på den ekstreme glathed på togskinner, når der er faldet løv på dem. I deres papir udgiv
Ingeniører finder ud af, hvorfor nedfaldne blade på togskinner er så glatteKredit:Pixabay/CC0 Public Domain Et team af ingeniører ved University of Sheffield har fundet en forklaring på den ekstreme glathed på togskinner, når der er faldet løv på dem. I deres papir udgiv -
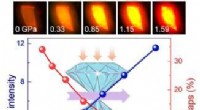 Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research
Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research -
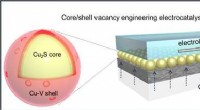 Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol
Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol -
 Materialeforskere finder en ny vinkel mod bedre varmeoverførselSilicium wafers belagt med gradient ENZ materialer set gennem et termisk billedkamera. Kredit:Raman Laboratory/UCLA UCLA-materialeforskere har udviklet en klasse af optisk materiale, der styrer, h
Materialeforskere finder en ny vinkel mod bedre varmeoverførselSilicium wafers belagt med gradient ENZ materialer set gennem et termisk billedkamera. Kredit:Raman Laboratory/UCLA UCLA-materialeforskere har udviklet en klasse af optisk materiale, der styrer, h
- De'shana vasker sin lastbil. Hun skal bruge i alt 10 liter for at fylde spanden. Vælg det udtryk, d…
- Taknemmelighed eller skyld? Folk bruger mere, når de 'betaler det frem'
- Involverer kemisk forvitring altid vand?
- Mystisk nanoboble brister?
- Hvis du blander madfarve og vand, gør det en kemisk reaktion?
- Når molekyler kommer tættere sammen, siges objektet til?


