Koncentrationen af både A og B blev også fordoblet reaktionshastigheden, hvad er loven for denne reaktion?
Forståelse af hastighedslove
* rate lov: Et matematisk udtryk, der beskriver, hvordan reaktionshastigheden afhænger af reaktanternes koncentrationer.
* Bestilling: Eksponenten for hver reaktants koncentration i satsens lov er dens rækkefølge.
analyse af informationen
Du får følgende:
* fordobling [a] og [b] fordobler satsen. Dette indebærer, at reaktionen er første orden Med hensyn til både A og B.
Skrivning af satsens lov
Baseret på oplysningerne er hastighedsloven for reaktionen:
hastighed =k [a] [b]
Hvor:
* k er hastigheden konstant
* [a] er koncentrationen af reaktant a
* [b] er koncentrationen af reaktant B
Forklaring
* første orden med hensyn til en: Hvis du fordobler [a], fordobles hastigheden.
* første orden med hensyn til B: Hvis du dobbelt [b], fordobles hastigheden.
overordnet ordre
Denne reaktion er anden ordre Samlet set fordi eksponenterne for koncentrationerne i hastighedsloven tilføjer op til 2 (1 + 1 =2).
 Varme artikler
Varme artikler
-
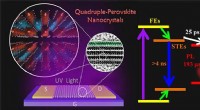 Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk
Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk -
 Sådan finder du molekylære lim til effektivt at målrette sygdommeNye strategier til små molekylære lim. Kredit:Eindhoven University of Technology Mange af de i øjeblikket tilgængelige lægemidler er ikke specifikke nok til effektivt at helbrede komplekse sygdomm
Sådan finder du molekylære lim til effektivt at målrette sygdommeNye strategier til små molekylære lim. Kredit:Eindhoven University of Technology Mange af de i øjeblikket tilgængelige lægemidler er ikke specifikke nok til effektivt at helbrede komplekse sygdomm -
 Forstå hvad der gør Tennessee whisky unikKredit:CC0 Public Domain Sukker ahorn træet giver efterårsløv, ahornsirup og Tennessee whisky. Træ fra træet hakkes i planker, stablet i bunker og brændt for at danne kul. Frisk destilleret, ikke-
Forstå hvad der gør Tennessee whisky unikKredit:CC0 Public Domain Sukker ahorn træet giver efterårsløv, ahornsirup og Tennessee whisky. Træ fra træet hakkes i planker, stablet i bunker og brændt for at danne kul. Frisk destilleret, ikke- -
 Kan fremtidens huse laves af bakterier?Et hus lavet af et plastik-lignende materiale skabt af bakterier i Neel Joshis laboratorium. Kredit:Ruby Wallau/Northeastern University Tænk, hvis vi kunne dyrke en bygning, som koralpolypper dyrk
Kan fremtidens huse laves af bakterier?Et hus lavet af et plastik-lignende materiale skabt af bakterier i Neel Joshis laboratorium. Kredit:Ruby Wallau/Northeastern University Tænk, hvis vi kunne dyrke en bygning, som koralpolypper dyrk
- Undersøgelse bekræfter stabil opvarmning af oceaner i de sidste 75 år
- Er en meter længere end 1000000000 nanometer?
- Astronomer løser mysteriet om hvide dværgmasser
- Hvilke af følgende metoder kan bruges til at bestemme temperatur en stjerne?
- Hvilken type binding omkring en central ville resultere i trigonalt plan molekyle -apex?
- Ny måling af universets ekspansionshastighed sidder fast i midten


