Hvad er massen på 1,505 x 10²³ carbonatomer?
1. Avogadros nummer
* Avogadros nummer er en grundlæggende konstant i kemi:6,022 x 10²³ atomer/mol. Dette betyder, at en mol af ethvert element indeholder 6,022 x 10²³ atomer.
2. Molmasse
* Den molære masse af kulstof er 12,01 g/mol. Dette betyder, at en mol carbonatomer vejer 12,01 gram.
3. Beregning
* Trin 1:Find antallet af mol:
Del antallet af atomer med Avogadros nummer:
(1,505 x 10²³ atomer) / (6,022 x 10²³ atomer / mol) =0,250 mol
* Trin 2:Beregn massen:
Multiplicer antallet af mol med den molære masse:
(0,250 mol) * (12,01 g/mol) =3,00 g
Derfor er massen på 1,505 x 10²³ carbonatomer 3,00 gram
Sidste artikelHvilken reaktion er dette et eksempel på 2 H2 O2 ----- H2O?
Næste artikelHvad er kobberoxider ph?
 Varme artikler
Varme artikler
-
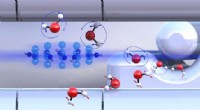 Sammenligning af vandisomerers kemiForsorterede ortho-vand- og para-vand-molekyler med forskelligt orienterede nukleare spins (blå eller røde pile) reagerer med diazenyliumioner (i midten til venstre) ved forskellige hastigheder. Kredi
Sammenligning af vandisomerers kemiForsorterede ortho-vand- og para-vand-molekyler med forskelligt orienterede nukleare spins (blå eller røde pile) reagerer med diazenyliumioner (i midten til venstre) ved forskellige hastigheder. Kredi -
 Forfalsket arganolie afdækket gennem ny analysemetodeKredit:CC0 Public Domain Forskere fra Quadram Institute har udviklet en ny måde at teste ægtheden af arganolie på, en af verdens dyreste spiseolier. I de seneste år, det er blevet eftertragtet
Forfalsket arganolie afdækket gennem ny analysemetodeKredit:CC0 Public Domain Forskere fra Quadram Institute har udviklet en ny måde at teste ægtheden af arganolie på, en af verdens dyreste spiseolier. I de seneste år, det er blevet eftertragtet -
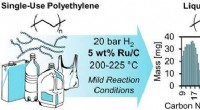 En mild måde at opgradere plastik brugt i flasker til brændstof og andre højværdiprodukterKredit:American Chemical Society Plast er allestedsnærværende i menneskers liv. Endnu, når plastholdige genstande har opfyldt deres missioner, kun en lille mængde genanvendes til nye produkter, so
En mild måde at opgradere plastik brugt i flasker til brændstof og andre højværdiprodukterKredit:American Chemical Society Plast er allestedsnærværende i menneskers liv. Endnu, når plastholdige genstande har opfyldt deres missioner, kun en lille mængde genanvendes til nye produkter, so -
 Video:Hvorfor har vi ikke syntetisk blod endnu?Kredit:The American Chemical Society Der doneres millioner af liter blod rundt om i verden hvert år, men der er stadig ikke nok til alle, der har brug for det. Kemikere har i et århundrede forsøgt
Video:Hvorfor har vi ikke syntetisk blod endnu?Kredit:The American Chemical Society Der doneres millioner af liter blod rundt om i verden hvert år, men der er stadig ikke nok til alle, der har brug for det. Kemikere har i et århundrede forsøgt
- Hvorfor er fedt en god opbevaringsenhed til energi?
- Troscentrerede tatoveringer analyseres i studiet af universitetsstuderende
- Hvorfor bruges bølgelængden 275 nm til at måle absorbans af koffein?
- 5 evidensbaserede måder, lærere kan hjælpe svære elever på
- Hvorfor en overraskende opdagelse, opvarmning af havene og 'Meg's død kan skabe problemer for flere…
- Hvilken slags stof er saccharose-forbindelse eller blanding?


