Hvilken væske har den laveste overfladespænding?
Her er hvorfor:
* overfladespænding er et mål for de sammenhængende kræfter mellem molekyler ved overfladen af en væske.
* diethylether har svage intermolekylære kræfter (van der Waals Forces) på grund af dens relativt lille størrelse og ikke-polære karakter. Dette betyder, at molekylerne ikke klæber sammen meget stærkt, hvilket resulterer i en lav overfladespænding.
Til sammenligning er her nogle andre væsker med relativt lave overfladespændinger:
* acetone
* hexan
* methanol
Det er vigtigt at bemærke, at overfladespænding er påvirket af temperaturen. Når temperaturen på en væske øges, falder dens overfladespænding.
Sidste artikelHvad skal en gas gå igennem og blive solid?
Næste artikelHvad udfører jeg meget godt?
 Varme artikler
Varme artikler
-
 Implanterbar piezoelektrisk polymer forbedrer kontrolleret frigivelse af lægemidlerEn implanterbar piezoelektrisk polymer nanofiber -enhed, der frigiver kontrollerede mængder af et lægemiddel under mekanisk kraft. Kredit:Jin Nam/UCR En membran lavet af tråde af en polymer, der a
Implanterbar piezoelektrisk polymer forbedrer kontrolleret frigivelse af lægemidlerEn implanterbar piezoelektrisk polymer nanofiber -enhed, der frigiver kontrollerede mængder af et lægemiddel under mekanisk kraft. Kredit:Jin Nam/UCR En membran lavet af tråde af en polymer, der a -
 Kunstig tunge kan skelne mellem whiskyKredit:University of Glasgow Forskere afslørede tirsdag, at de er kommet med en kunstig tunge, der kan skelne subtile forskelle mellem whisky. Eksperter ved University of Glasgow har bygget miniat
Kunstig tunge kan skelne mellem whiskyKredit:University of Glasgow Forskere afslørede tirsdag, at de er kommet med en kunstig tunge, der kan skelne subtile forskelle mellem whisky. Eksperter ved University of Glasgow har bygget miniat -
 Kemikalier, der helbreder malaria, kan også dræbe ukrudtPlantebiologer ved University of Western Australia har afsløret forholdet mellem planter og parasitten, der forårsager malaria, er tæt nok til at betyde, at mange lægemidler mod malaria er effektive h
Kemikalier, der helbreder malaria, kan også dræbe ukrudtPlantebiologer ved University of Western Australia har afsløret forholdet mellem planter og parasitten, der forårsager malaria, er tæt nok til at betyde, at mange lægemidler mod malaria er effektive h -
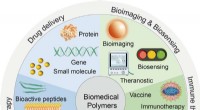 Biomedicinske polymerer:syntese, egenskaber og anvendelserSkematisk illustration af smarte polymerer til biomedicinske applikationer. Kredit:Science China Press Biomedicinske polymerer er blevet omfattende udviklet til lovende anvendelser inden for en mas
Biomedicinske polymerer:syntese, egenskaber og anvendelserSkematisk illustration af smarte polymerer til biomedicinske applikationer. Kredit:Science China Press Biomedicinske polymerer er blevet omfattende udviklet til lovende anvendelser inden for en mas
- Hvad er en sedimentær klippe, der består af fragmenter med runde kanter kaldet?
- Faktorer, der påvirker et valgsted til en vandkraftstation
- Hvordan nerveceller kontrollerer fejlfoldede proteiner
- Spanien Bilbao kæmper for at lede europæisk vindkraftsektor
- Dybtgående splittelser i Storbritannien afsløret af Brexit-undersøgelse
- Spion-satellitbilleder fra koldkrigstiden afslører mulige virkninger af klimaændringer


