Udført, hvad den nukleare model af atom indikerer om volumen i atom.?
1. Nucleus er lille og tæt:
* lille: Kernen, der indeholder protoner og neutroner, optager et utroligt lille volumen sammenlignet med atomets samlede størrelse. Forestil dig et stadion med en marmor i midten - marmoren repræsenterer kernen, og stadionet repræsenterer atomet.
* Tæt: På trods af sin lille størrelse indeholder kernen næsten al masse af atomet. Dette skyldes, at protoner og neutroner er meget tungere end elektroner. Denne ekstreme tæthed gør kernen det tætteste kendte stof.
2. Det meste af atomet er tomt rum:
* Langt de fleste af et atomvolumen besættes af de elektroner, der kredser om kernen. Disse elektroner er i konstant bevægelse omkring kernen og skaber en diffus sky af negativ ladning.
* Dette "tomme rum" er ikke rigtigt tomt. Det er her sandsynligheden for at finde en elektron er højest. Det volumen, der er optaget af elektroner, er enorm sammenlignet med kernen, hvilket gør atomet for det meste tomme rum.
3. Volumen bestemmes af elektroniske orbitaler:
* Størrelsen på et atom bestemmes primært af størrelsen og formen af de elektroniske orbitaler, der omgiver kernen. Disse orbitaler er områder af plads, hvor sandsynligheden for at finde en elektron er højest.
* Forskellige elementer har forskellige elektronkonfigurationer og derfor forskellige orbitalstørrelser. Dette forklarer, hvorfor atomer af forskellige elementer har forskellige atomradier.
I resumé understreger den nukleare model, at det meste af et atomvolumen er tomt rum. Dette er en direkte konsekvens af, at den lille, tætte kerne er omgivet af en meget større, diffus sky af elektroner.
implikationer:
* Kemiske reaktioner: Det tomme rum i atomer spiller en afgørende rolle i kemiske reaktioner. Atomer kan dele eller overføre elektroner med andre atomer, hvilket resulterer i dannelse af molekyler. Atomets volumen muliggør denne interaktion.
* Forståelse Materiale: Den nukleare model hjælper med at forklare materialerne ved stof. For eksempel bidrager det enorme tomme rum i atomer til komprimerbarheden af gasser.
Det er vigtigt at huske, at den nukleare model, selvom den er vellykket, er en forenkling. Den faktiske opførsel af elektroner er mere kompleks end beskrevet i denne model. Det er dog stadig et grundlæggende fundament for vores forståelse af atomstruktur og materiens art.
 Varme artikler
Varme artikler
-
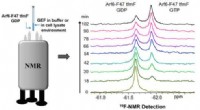 Hurtig metode hjælper med at detektere Arf6 guanin nukleotid udvekslingsfaktor aktivitet19 F NMR-baseret metode til Arf6 GEF aktivitet detektion. Kredit:Wu Bo Et forskerhold ledet af prof. Wang Junfeng fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabsakad
Hurtig metode hjælper med at detektere Arf6 guanin nukleotid udvekslingsfaktor aktivitet19 F NMR-baseret metode til Arf6 GEF aktivitet detektion. Kredit:Wu Bo Et forskerhold ledet af prof. Wang Junfeng fra Hefei Institutes of Physical Science (HFIPS) under det kinesiske videnskabsakad -
 Ny teknologi konverterer plastaffald til jetbrændstof på en timeKredit:CC0 Public Domain Washington State University-forskere har udviklet en innovativ måde at omdanne plastik til ingredienser til jetbrændstof og andre værdifulde produkter, gør det nemmere og
Ny teknologi konverterer plastaffald til jetbrændstof på en timeKredit:CC0 Public Domain Washington State University-forskere har udviklet en innovativ måde at omdanne plastik til ingredienser til jetbrændstof og andre værdifulde produkter, gør det nemmere og -
 Oprettelse af materialer på en ny måde ved hjælp af 3D-trykbakterierKredit:ACS (Phys.org) – Et team af forskere ved Delft University of Technology har udviklet et middel til 3D-print af en gel indeholdende bakterier på en base for at skabe materialer på en ny måde
Oprettelse af materialer på en ny måde ved hjælp af 3D-trykbakterierKredit:ACS (Phys.org) – Et team af forskere ved Delft University of Technology har udviklet et middel til 3D-print af en gel indeholdende bakterier på en base for at skabe materialer på en ny måde -
 Kemikeres gennembrud i syntese fremmer et potent anti-kræftmiddelVi brugte årtier på grundforskning og gjorde meget dramatiske fremskridt, sagde Yoshito Kishi, Morris Loeb, professor i kemi, Emeritus, i Harvards afdeling for kemi og kemisk biologi. Kredit:Stephanie
Kemikeres gennembrud i syntese fremmer et potent anti-kræftmiddelVi brugte årtier på grundforskning og gjorde meget dramatiske fremskridt, sagde Yoshito Kishi, Morris Loeb, professor i kemi, Emeritus, i Harvards afdeling for kemi og kemisk biologi. Kredit:Stephanie
- Hvad er et eksempel på lyd energi til elektrisk energi?
- Forskere kaster sig ud i havets skumringszone for at udforske økosystemets kulstofstrøm
- Den specifikke guldvarme er 0,131 joules pr. Gram. Celsius Hvor meget energi kræves til 1,3 gram fr…
- Videnskabseksperimenter med tennisbolde
- Hvorfor ansvarlig indkøb af DRC-mineraler har store svage punkter
- Hvilket underlag fungerer spytamylase på?


