Er svovl en god leder af elektrisitet?
Her er hvorfor:
* atomstruktur: Svovlatomer har et stærkt greb på deres elektroner, hvilket gør dem tilbageholdende med let at bevæge sig og bære en elektrisk strøm. Dette skyldes svovlens position i den periodiske tabel som en ikke -metal og dens høje elektronegativitet.
* Mangel på frie elektroner: I modsætning til metaller, der har et "hav" af frie elektroner, har svovl meget få frie elektroner. Dette gør det vanskeligt for elektricitet at flyde gennem det.
* isolerende egenskaber: Svovl er faktisk en god isolator, hvilket betyder, at den modstår strømmen af elektricitet. Denne egenskab bruges i forskellige applikationer, såsom elektrisk isolering i transformere og højspændingsudstyr.
Kortfattet , svovls atomstruktur og mangel på frie elektroner gør det til en dårlig leder af elektricitet.
Sidste artikelHvilke reaktioner producerer elektroner?
Næste artikelHvordan bestemmer du valenselektroner ved hjælp af orbitaldiagram?
 Varme artikler
Varme artikler
-
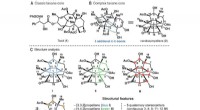 Endelig syntetisk canataxpropellan:Reproducerer et af naturens mest komplekse produkterSammenligning af Taxol-kernen med den komplekse taxankerne og nøgletræk ved (–)-canataxpropellane (2). Kredit: Videnskab (2020). DOI:10.1126/science.aay9173 Et team af kemikere ved universitetet
Endelig syntetisk canataxpropellan:Reproducerer et af naturens mest komplekse produkterSammenligning af Taxol-kernen med den komplekse taxankerne og nøgletræk ved (–)-canataxpropellane (2). Kredit: Videnskab (2020). DOI:10.1126/science.aay9173 Et team af kemikere ved universitetet -
 En ikke-destruktiv metode til at analysere oldægyptiske balsameringsmaterialerForskere analyserede balsameringsmateriale fra halsen på denne gamle egyptiske mumie, som blev erhvervet af et fransk museum i 1837. Kredit:Frédérique Vincent, etnografisk konservator Gamle egypti
En ikke-destruktiv metode til at analysere oldægyptiske balsameringsmaterialerForskere analyserede balsameringsmateriale fra halsen på denne gamle egyptiske mumie, som blev erhvervet af et fransk museum i 1837. Kredit:Frédérique Vincent, etnografisk konservator Gamle egypti -
 Øjeblikkelig vandrensningsmetode millioner af gange bedre end kommerciel tilgangKredit:Pixabay/CC0 Public Domain Et vanddesinfektionsmiddel, der er skabt på stedet ved hjælp af kun brint og luften omkring os, er millioner af gange mere effektivt til at dræbe vira og bakterier
Øjeblikkelig vandrensningsmetode millioner af gange bedre end kommerciel tilgangKredit:Pixabay/CC0 Public Domain Et vanddesinfektionsmiddel, der er skabt på stedet ved hjælp af kun brint og luften omkring os, er millioner af gange mere effektivt til at dræbe vira og bakterier -
 Fødevareforskere sigter mod at gøre plantebaseret protein smagere og sundereDavid Julian McClements er en fremtrædende professor i fødevarevidenskab ved UMass Amherst. Kredit:UMass Amherst I takt med at kødspisningen fortsætter med at stige rundt om i verden, fødevarefors
Fødevareforskere sigter mod at gøre plantebaseret protein smagere og sundereDavid Julian McClements er en fremtrædende professor i fødevarevidenskab ved UMass Amherst. Kredit:UMass Amherst I takt med at kødspisningen fortsætter med at stige rundt om i verden, fødevarefors
- Hvad bruges videnskabelig forskning til?
- FAST hjælper med at afsløre oprindelsen af hurtige radioudbrud
- Forskere opnår verdens første manipulation af antistof med laser
- Hvordan coronavirus har ændret luftkvaliteten, og hvad det kan betyde for vejret
- Hvilken hjernekerne er det biologiske ur?
- Hvad er energikonvertering i et batterilommelygte?


