Hvordan gør en hypotonisk løsning til en isotonisk løsning?
* Hypotonisk vs. isotonisk:
* hypotonisk: En opløsning med en lavere opløst stofkoncentration sammenlignet med en anden opløsning (som en celle). Vand bevæger sig ind i den hypotoniske opløsning for at forsøge at udligne koncentrationer.
* isotonisk: En opløsning med den samme opløste koncentration som en anden løsning. Der er ingen nettobevægelse af vand.
* gør det isotonisk:
* Tilføjelse af opløste stoffer: Ved at øge den opløste koncentration af den hypotoniske opløsning bringer du den tættere på koncentrationen af den løsning, du sammenligner den med. Dette reducerer forskellen i opløst koncentration, hvilket gør opløsningen mere isotonisk.
Her er et praktisk eksempel:
1. Forestil dig, at du har en hypotonisk opløsning af destilleret vand (0% opløst koncentration). Du vil gøre det isotonisk til en celles cytoplasma (ca. 0,9% opløst koncentration).
2. For at gøre det isotonisk vil du tilføje et opløst stof, såsom salt (NaCl), til det destillerede vand. Du vil gradvist tilsætte salt, indtil koncentrationen af vandopløsningen når 0,9%.
Vigtige overvejelser:
* type opløst stof: Den type opløst stof, du bruger, betyder noget. Du har brug for et opløst stof, der ikke vil skade cellerne eller forårsage andre uønskede reaktioner.
* Specifik løsning: Den nøjagtige mængde opløst stof, du har brug for for at tilføje, afhænger af den indledende koncentration af den hypotoniske opløsning og den ønskede isotoniske koncentration.
* applikationer: Denne proces bruges i forskellige applikationer, såsom:
* IV -løsninger: Intravenøse opløsninger skal være isotonisk for blodet for at undgå at beskadige røde blodlegemer.
* Cellekultur: Celler dyrkes i isotoniske medier for at sikre deres rette funktion og overlevelse.
Husk: Vær altid forsigtig, når du arbejder med løsninger, og konsulter pålidelige kilder for nøjagtige oplysninger.
 Varme artikler
Varme artikler
-
 Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering
Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering -
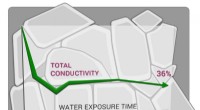 Forskere viser, at en lovende fast elektrolyt er hydrofobSkoltech-forskere og deres kolleger har vist, at LATP, en fast elektrolyt, der overvejes til brug i næste generations energilagring, er meget følsom over for vand, hvilket har direkte konsekvenser for
Forskere viser, at en lovende fast elektrolyt er hydrofobSkoltech-forskere og deres kolleger har vist, at LATP, en fast elektrolyt, der overvejes til brug i næste generations energilagring, er meget følsom over for vand, hvilket har direkte konsekvenser for -
 At forme proteiner for at forstå chaperone-relaterede sygdommeKredit:Leiden Universitet Chaperones er et sæt proteiner, der er specialiseret til at hjælpe proteiner i den menneskelige krop. De hjælper proteiner med at folde sig til den rigtige form og beskyt
At forme proteiner for at forstå chaperone-relaterede sygdommeKredit:Leiden Universitet Chaperones er et sæt proteiner, der er specialiseret til at hjælpe proteiner i den menneskelige krop. De hjælper proteiner med at folde sig til den rigtige form og beskyt -
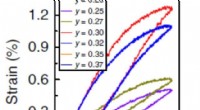 Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill
Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill
- El Nino ændrer geografisk fordeling af koleratilfælde i Afrika
- Har en leder uendelig kapacitet?
- Voksende bioinspirerede former med hundredvis af små robotter
- Ris, Penn State åbent center for 2-D belægninger
- Kan du udarbejde hastigheden på et objekt ved at bruge masse og afstand?
- Afromontane skove og klimaændringer


