Atomer fyldt med yderste energiniveauer har tendens til, hvad de skal deltage i kemiske reaktioner?
* stabilitet: Atomer med fuldt yderste energiniveau (som ædelgasser) er utroligt stabile. De har en afbalanceret og komplet elektronkonfiguration, hvilket gør dem tilbageholdende med at vinde eller miste elektroner.
* inertness: Denne stabilitet fører til, at de er inert, hvilket betyder, at de ikke let danner kemiske bindinger med andre atomer.
Eksempel: Helium (HE) har en fuld yderste skal med 2 elektroner. Det deltager sjældent i kemiske reaktioner.
Undtagelser: Nogle elementer med fyldte yderste skaller kan deltage i reaktioner under meget specifikke forhold. Disse reaktioner involverer ofte høj energi eller dannelse af usædvanlige bindingsmønstre.
I modsætning: Atomer med delvist fyldte yderste energiniveauer er mere tilbøjelige til at reagere og søger at vinde eller miste elektroner for at opnå en stabil konfiguration.
 Varme artikler
Varme artikler
-
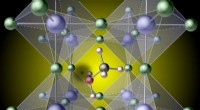 Brint i hybridperovskiter er mindre uskyldigt, end det ser udEn brinttomgang (den sorte plet til venstre for midten) skabt ved at fjerne brint fra et methylammoniummolekyle, fanger bærere i den prototypiske hybridperovskit, mehtylammonium blyiodid CH3NH3Pbl3. K
Brint i hybridperovskiter er mindre uskyldigt, end det ser udEn brinttomgang (den sorte plet til venstre for midten) skabt ved at fjerne brint fra et methylammoniummolekyle, fanger bærere i den prototypiske hybridperovskit, mehtylammonium blyiodid CH3NH3Pbl3. K -
 Ny katalysator til elektrokemisk selektiv C=O-hydrogenering af kanelaldehydHRTEM og elementær kortlægningsresultater af Pt-MoO3 /C. Kredit:Wang Jialu Forskere fra Institute of Solid State Physics, Hefei Institutes of Physical Science ved det kinesiske videnskabsakademi, r
Ny katalysator til elektrokemisk selektiv C=O-hydrogenering af kanelaldehydHRTEM og elementær kortlægningsresultater af Pt-MoO3 /C. Kredit:Wang Jialu Forskere fra Institute of Solid State Physics, Hefei Institutes of Physical Science ved det kinesiske videnskabsakademi, r -
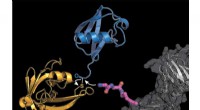 Mærkning af proteiner med ubiquitin baner ny vej til forskning i cellereguleringForskerne udstyrede et cellulært protein (gråt) med en modificeret lysinaminosyre byggesten (lyserød), hvortil det bakterielle enzym sortase (gul) transmitterer et ubiquitinmolekyle (blåt). Kredit:K.
Mærkning af proteiner med ubiquitin baner ny vej til forskning i cellereguleringForskerne udstyrede et cellulært protein (gråt) med en modificeret lysinaminosyre byggesten (lyserød), hvortil det bakterielle enzym sortase (gul) transmitterer et ubiquitinmolekyle (blåt). Kredit:K. -
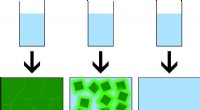 Mysteriet om amorf perovskit løstIllustrationen viser, at jo mere methylammoniumacetat (MAAc) vi tilsætter, jo mindre orden ser vi i vores materiale. Dette spænder fra fuldt krystallinsk, i grøn, til amorf med krystallinsk, meget lys
Mysteriet om amorf perovskit løstIllustrationen viser, at jo mere methylammoniumacetat (MAAc) vi tilsætter, jo mindre orden ser vi i vores materiale. Dette spænder fra fuldt krystallinsk, i grøn, til amorf med krystallinsk, meget lys
- Kemikalier fra landmændsfelter, hvor flyder de evntuelt?
- MRNA er nødvendigt for at syntetisere, hvad i cytoplasmaet?
- Brug af slamorm som model for aktive filamenter i viskositetstest
- Hvordan så de første slanger ud?
- Genomisk undersøgelse udforsker udviklingen af blide dræberbier i Puerto Rico
- Beskriv kort bevægelse af partikler i kobber?


