Forståelse af jernkorrosion:Videnskaben om rustdannelse
Korrosion af jern i fugtig luft:En detaljeret forklaring
Korrosionen af jern i fugtig luft, almindeligvis kendt som rustning, er en kompleks elektrokemisk proces, der involverer flere trin:
1. Dannelse af en elektrolyt:
* Fugtig luft indeholder opløst ilt og kuldioxid.
* Dette skaber et tyndt lag elektrolyt (en opløsning, der leder elektricitet) på jernoverfladen.
2. Dannelse af anodiske og katodiske steder:
* Jern er ikke helt ensartet. Der er små variationer i dens sammensætning og struktur.
* Dette fører til dannelsen af anodiske websteder (hvor oxidation forekommer) og katodiske steder (hvor der sker reduktion) på jernoverfladen.
3. Oxidation ved anoden:
* På de anodiske steder mister jernatomer elektroner og danner jernioner (Fe²⁺):
* Fe(r) → Fe²⁺(aq) + 2e⁻
* Disse jernioner reagerer derefter med ilt og vand for at danne hydreret jern(II)oxid:
* Fe²⁺(aq) + 2OH⁻(aq) → Fe(OH)₂(s)
4. Reduktion ved katoden:
* På de katodiske steder optager opløst oxygen i elektrolytten elektroner og reagerer med vand for at danne hydroxidioner (OH⁻):
* O₂(vandig) + 2H2O(l) + 4e⁻ → 4OH⁻(vandig)
5. Dannelse af rust:
* Det hydrerede jern(II)oxid (Fe(OH)₂) reagerer yderligere med oxygen og vand for at danne hydreret jern(III)oxid, almindeligvis kendt som rust (Fe₂O₃.xH₂O):
* 4Fe(OH)2(s) + O2(g) → 2Fe2O3.xH2O(s) + 2H2O(l)
Faktorer, der påvirker rust:
* Tilstedeværelse af vand: Fugt er afgørende for dannelsen af elektrolytten, hvilket gør rusten mere fremtrædende i fugtige omgivelser.
* Tilstedeværelse af ilt: Ilt fungerer som et oxidationsmiddel, der accelererer korrosionsprocessen.
* Surhed: Sure miljøer (som dem med opløst kuldioxid) fremskynder processen ved at øge elektrolyttens ledningsevne og hjælpe med dannelsen af jernioner.
* Temperatur: Højere temperaturer øger reaktionshastighederne, hvilket fører til hurtigere korrosion.
* Tilstedeværelse af elektrolytter: Andre opløste salte og mineraler i vand kan fungere som elektrolytter og øge korrosion.
* Overfladetilstand: Ru eller beskadigede overflader giver flere steder, hvor processen kan starte.
Forebyggelse af rust:
* Belægning: Påføring af maling, olie eller andre beskyttende belægninger forhindrer ilt og fugt i at nå jernoverfladen.
* Galvanisering: At dække jern med et lag zink beskytter det ved at fungere som en offeranode. Zink korroderer i stedet for jern, hvilket effektivt beskytter det underliggende metal.
* Legering: At skabe legeringer som rustfrit stål inkorporerer elementer, der modstår korrosion.
* Katodisk beskyttelse: Fastgøring af et mere reaktivt metal til jernoverfladen for at fungere som en offeranode.
Konsekvenser af rust:
* Rust svækker jernstrukturen og kan i sidste ende forårsage svigt.
* Det kan føre til betydelige økonomiske tab på grund af skader på strukturer og maskiner.
* Det giver miljøproblemer på grund af frigivelse af jern til miljøet.
At forstå rustmekanismen er afgørende for at udvikle strategier til at forhindre det og bevare integriteten af jernbaserede materialer.
Sidste artikelFosfor- og svovlbinding:Kovalent binding forklaret
Næste artikelHvorfor opløst salt er usynligt:Videnskaben forklaret
 Varme artikler
Varme artikler
-
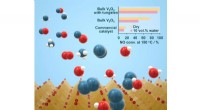 Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox
Wolframsubstitueret vanadiumoxid indånder frisk luft i katalysatorteknologiIllustration af ammoniak og nitrogenoxidmolekyler over et krystallinsk katalytisk materiale. (indsat) Kvælstofoxidkonverteringshastigheder ved 150 grader Celsius for wolframsubstitueret bulkvanadiumox -
 Forskere udvikler nye, hurtig pipeline for antimikrobielle stofferASU-forskere har for nylig mødt en udfordring med at udvikle en ny klasse af antimikrobielle stoffer, kaldet synbodies, at beskytte befolkningen mod smitsomme trusler - alt sammen inden for en uge. Kr
Forskere udvikler nye, hurtig pipeline for antimikrobielle stofferASU-forskere har for nylig mødt en udfordring med at udvikle en ny klasse af antimikrobielle stoffer, kaldet synbodies, at beskytte befolkningen mod smitsomme trusler - alt sammen inden for en uge. Kr -
 Beregning af vindbelastninger ud fra vindhastigheder:En praktisk vejledning for ingeniørerAf Lee Johnson, Opdateret 24. marts 2022 Alle udendørs strukturer skal være konstrueret til at modstå vindstyrker. Selvom den grundlæggende fysik er enkel, kræver design i den virkelige verden omhygg
Beregning af vindbelastninger ud fra vindhastigheder:En praktisk vejledning for ingeniørerAf Lee Johnson, Opdateret 24. marts 2022 Alle udendørs strukturer skal være konstrueret til at modstå vindstyrker. Selvom den grundlæggende fysik er enkel, kræver design i den virkelige verden omhygg -
 Gamle proteiner giver spor til fortidenKredit:CC0 Public Domain Arkæologer stolede engang udelukkende på artefakter, såsom skeletrester, fossiler og keramikskår, at lære om tidligere arter og kulturer. Nutidens videnskabsmænd kan også
Gamle proteiner giver spor til fortidenKredit:CC0 Public Domain Arkæologer stolede engang udelukkende på artefakter, såsom skeletrester, fossiler og keramikskår, at lære om tidligere arter og kulturer. Nutidens videnskabsmænd kan også
- Forskere opdager manglende ingrediens fra jordens kontinentale skorpe
- Urolige farvande:Kina-drevet krydstogtboom vækker frygt for miljøet
- Er smeltet kobber et mineral hvorfor eller ej?
- I mediernes dækning af klimaændringer, hvor er fakta?
- Sådan tilføjes og trækkes Negative Fractions
- Arabisk rumfartøj lukker ind på Mars på en historisk flyvning


