Elektrontab i hovedgruppemetaller:s-orbitaler vs. d-orbitaler
* Elektronkonfiguration: Hovedgruppemetaller har deres valenselektroner i s- og p-orbitaler. d-underskallen er fyldt før s- og p-orbitaler i perioden 4 overgangsmetaller, men den er ikke en del af valenselektronkonfigurationen for hovedgruppemetaller.
* Ioniseringsenergi: Ioniseringsenergien (den energi, der kræves for at fjerne en elektron) er generelt lavere for s-elektroner end for d-elektroner. Dette skyldes, at s-elektroner er længere væk fra kernen og oplever mindre effektiv nuklear ladning (tiltrækningen mellem kernen og elektronerne).
* Stabilitet: At miste elektroner fra s subshell fører til en mere stabil elektronkonfiguration for hovedgruppemetaller, da de sigter mod at opnå en ædelgaskonfiguration.
Eksempel: Tin (Sn) har elektronkonfigurationen [Kr] 4d¹⁰ 5s² 5p². Når den danner en kation, mister den først de to 5p-elektroner, efterfulgt af de to 5s-elektroner.
Vigtig bemærkning: Mens hovedgruppemetaller ikke mister d-elektroner først, kan de have d-orbitaler involveret i binding. For eksempel kan Sn danne Sn²⁺- eller Sn⁴⁺-ioner, men det kan også deltage i kovalent binding ved hjælp af dets d-orbitaler.
Sammenfattende er tendensen hos hovedgruppemetaller at miste elektroner fra deres s og p subshells først, ikke d subshell.
 Varme artikler
Varme artikler
-
 Nikkelkatalysator letter oprettelsen af en enkelt stereoisomer med to kirale centreAlkyl-alkylbindingsdannelse. (A) Katalysatorstyret stereoselektivitet-tidligere arbejde. (B) Katalysatorstyret stereoselektivitet-denne undersøgelse. ee, enantiomert overskud; M, metal; R, substituent
Nikkelkatalysator letter oprettelsen af en enkelt stereoisomer med to kirale centreAlkyl-alkylbindingsdannelse. (A) Katalysatorstyret stereoselektivitet-tidligere arbejde. (B) Katalysatorstyret stereoselektivitet-denne undersøgelse. ee, enantiomert overskud; M, metal; R, substituent -
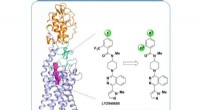 Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers
Forskere dechifrerer multi-domænet, struktur i fuld længde af den menneskelige glattede receptorStruktur af multi-domæne human Smoothened receptor, et vigtigt lægemiddelmål for kræftsygdomme. Kredit:ShanghaiTech University Et team af forskere ledet af iHuman Institute of ShanghaiTech Univers -
 Forskere adskiller protein-nanopartikel-interaktioner, foreslå vej til lægemiddel-sensing værktø…Arbejde fra videnskabsmænd ved Rice og Stanford universiteter afslørede, at bovint serumalbuminproteiner får guld nanorods til at danne højrehåndede chirale samlinger, mens de producerer chirale plasm
Forskere adskiller protein-nanopartikel-interaktioner, foreslå vej til lægemiddel-sensing værktø…Arbejde fra videnskabsmænd ved Rice og Stanford universiteter afslørede, at bovint serumalbuminproteiner får guld nanorods til at danne højrehåndede chirale samlinger, mens de producerer chirale plasm -
 Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk
Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk
- Hvad er betydningen af den nederste halvmåne i astrologi, og hvordan påvirker det vores daglige …
- Bevaringsopkald på planteskole med savfisk
- Sådan konverteres SCFM til NM3
- Plantenomenklatur:Hvordan navne afslører plantens udseende
- Hvorfor danner svovldioxid en sur opløsning?
- Forskning viser, hvordan tranebærjuice bekæmper bakterier på molekylært niveau


