Natriumklorid vs. sukker:Forståelse af elektrisk ledningsevne
Natriumchlorid (NaCl):
* Ionisk forbindelse: Natriumchlorid er en ionisk forbindelse. Det betyder, at det er dannet af den elektrostatiske tiltrækning mellem positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-).
* Dissociation i vand: Når natriumchlorid opløses i vand, brydes ionbindingerne, og ionerne bliver omgivet af vandmolekyler. Disse ioner er nu frie til at bevæge sig uafhængigt i løsningen.
* Konduktivitet: Tilstedeværelsen af frie, mobile ioner gør det muligt for løsningen at lede elektricitet. Når et elektrisk potentiale påføres, bevæger de positivt ladede ioner sig mod den negative elektrode (katode), og de negativt ladede ioner bevæger sig mod den positive elektrode (anode). Denne ladningsstrøm udgør en elektrisk strøm.
Sukker (saccharose):
* Kovalent forbindelse: Sukker er en kovalent forbindelse. Dens atomer holdes sammen af delte elektroner og danner stærke, neutrale molekyler.
* Ingen frie ioner: Når sukker opløses i vand, nedbrydes det ikke til ioner. Sukkermolekylerne forbliver intakte og bærer ikke elektrisk ladning.
* Ingen ledningsevne: Da der ikke er frie ioner til at bære ladningen, leder en sukkeropløsning ikke elektricitet.
Opsummering:
En løsnings evne til at lede elektricitet afhænger af tilstedeværelsen af frie, mobile ioner. Ioniske forbindelser som natriumchlorid dissocieres til ioner i opløsning, hvilket giver mulighed for ledningsevne. Kovalente forbindelser som sukker danner ikke ioner i opløsning og leder derfor ikke elektricitet.
 Varme artikler
Varme artikler
-
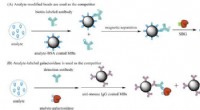 Ny immunoassay-teknik måler ekstremt lave koncentrationer af små molekyler ved hjælp af enkelt-mo…Skematisk illustration af konkurrerende Simoa-assays ved anvendelse af analytmodificerede MBer (A) og analyt-mærket β-galactosidase som konkurrent (B). Kredit:(c) Journal of the American Chemical Soc
Ny immunoassay-teknik måler ekstremt lave koncentrationer af små molekyler ved hjælp af enkelt-mo…Skematisk illustration af konkurrerende Simoa-assays ved anvendelse af analytmodificerede MBer (A) og analyt-mærket β-galactosidase som konkurrent (B). Kredit:(c) Journal of the American Chemical Soc -
 Hvorfor Epsom-salte opløses helt i vand, men kun delvist i spritAf Claire Gillespie Opdateret 24. marts 2022 Diane Macdonald/iStock/GettyImages Mens Epsom-salte ofte er parret med sprit til hjemmemedicin, bestemmer kemien bag blandingen, hvor effektiv den virkel
Hvorfor Epsom-salte opløses helt i vand, men kun delvist i spritAf Claire Gillespie Opdateret 24. marts 2022 Diane Macdonald/iStock/GettyImages Mens Epsom-salte ofte er parret med sprit til hjemmemedicin, bestemmer kemien bag blandingen, hvor effektiv den virkel -
 Ny teknik muliggør hurtig screening for nye typer solcellerDenne eksperimentelle opsætning blev brugt af holdet til at måle det elektriske output af en prøve af solcellemateriale, under kontrollerede forhold med varierende temperatur og belysning. Dataene fra
Ny teknik muliggør hurtig screening for nye typer solcellerDenne eksperimentelle opsætning blev brugt af holdet til at måle det elektriske output af en prøve af solcellemateriale, under kontrollerede forhold med varierende temperatur og belysning. Dataene fra -
 Selvbærende sløjfe af kemiske reaktioner kan revolutionere lægemiddelproduktionenEksperter fra University of Nottingham har skabt et selvbærende kredsløb af reaktioner, som er en grønnere og mere effektiv metode til kemisk produktion. offentliggjort i Nature Catalysis, Drs. France
Selvbærende sløjfe af kemiske reaktioner kan revolutionere lægemiddelproduktionenEksperter fra University of Nottingham har skabt et selvbærende kredsløb af reaktioner, som er en grønnere og mere effektiv metode til kemisk produktion. offentliggjort i Nature Catalysis, Drs. France
- NASA tager kraftig orkan Sergios temperatur
- Hvad er en imaginær linje trukket gennem Jorden fra nord til sydpol?
- I kølvandet på skovbrande og coronavirus, det er på tide, vi taler om menneskelig sikkerhed
- Hvilke typer celler har en cellemembrancytoplasma og kerne?
- Hvilket navn bruges til at beskrive organismer, der udfører fotosyntesen, gør deres egen mad?
- Sund jord er den virkelige nøgle til at brødføde verden


