Identifikation af elementer for ikke-polære kovalente bindinger:En guide
Her er hvorfor:
* Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner i en binding.
* Ikke-polære kovalente bindinger opstår, når de to atomer i bindingen deler elektroner ligeligt. Dette sker, når atomerne har lignende elektronegativitetsværdier, hvilket betyder, at de begge trækker på de delte elektroner med nogenlunde samme kraft.
Her er nogle eksempler på par af elementer, der højst sandsynligt ville danne ikke-polære kovalente bindinger:
* H - H (Brintgas):Begge brintatomer har samme elektronegativitet.
* Cl - Cl (Chlorgas):Begge kloratomer har samme elektronegativitet.
* C - C (Kulstof-kulstofbindinger i organiske molekyler):Kulstof har en relativt høj elektronegativitet, men da det binder med sig selv, er elektronegativitetsforskellen minimal.
* N - N (Nitrogengas):Begge nitrogenatomer har samme elektronegativitet.
Vigtig bemærkning: Selv elementer med lignende elektronegativitetsværdier kan nogle gange danne polære bindinger, hvis den molekylære geometri er asymmetrisk. For eksempel har vand (H2O) to polære bindinger mellem brint og oxygen, selvom elektronegativitetsforskellen mellem disse elementer er relativt lille.
 Varme artikler
Varme artikler
-
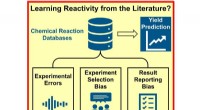 Hvor tydeligere rapportering af negative eksperimentelle resultater ville forbedre reaktionsplanlæg…Kredit:Angewandte Chemie Databaser indeholdende enorme mængder eksperimentelle data er tilgængelige for forskere på tværs af en lang række kemiske discipliner. Et team af forskere har imidlertid op
Hvor tydeligere rapportering af negative eksperimentelle resultater ville forbedre reaktionsplanlæg…Kredit:Angewandte Chemie Databaser indeholdende enorme mængder eksperimentelle data er tilgængelige for forskere på tværs af en lang række kemiske discipliner. Et team af forskere har imidlertid op -
 Målrettet jernoptagelse for at skabe en ny klasse af antibiotika mod UTI'erEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Med 11 millioner sager årligt, urinvejsinfektioner (UTIer) er de mest almindelige ambulante infektioner i USA, ifølge det amerikans
Målrettet jernoptagelse for at skabe en ny klasse af antibiotika mod UTI'erEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Med 11 millioner sager årligt, urinvejsinfektioner (UTIer) er de mest almindelige ambulante infektioner i USA, ifølge det amerikans -
 Ny forskning afslører hemmelighederne bag fotosyntesen, der kan hjælpe med at udvikle computertekn…Illustrerer, hvordan destinationen for en elektron (repræsenteret af toget) kan dirigeres efter påføring af en ultrahurtig mid-infrarød puls (repræsenteret af ilden). Kredit:Helen Towrie ved CLF F
Ny forskning afslører hemmelighederne bag fotosyntesen, der kan hjælpe med at udvikle computertekn…Illustrerer, hvordan destinationen for en elektron (repræsenteret af toget) kan dirigeres efter påføring af en ultrahurtig mid-infrarød puls (repræsenteret af ilden). Kredit:Helen Towrie ved CLF F -
 Solceller:Kortlægning af landskabet for cæsiumbaserede uorganiske halogenidperovskitterAlle prøver er blevet udskrevet i HySPRINT-laboratoriet på HZB. Kredit:H. Näsström/HZB Forskere ved HZB har trykt og undersøgt forskellige sammensætninger af cæsiumbaserede halogenidperovskitter (
Solceller:Kortlægning af landskabet for cæsiumbaserede uorganiske halogenidperovskitterAlle prøver er blevet udskrevet i HySPRINT-laboratoriet på HZB. Kredit:H. Näsström/HZB Forskere ved HZB har trykt og undersøgt forskellige sammensætninger af cæsiumbaserede halogenidperovskitter (
- Nyt materiale til at overgå traditionelle oxygenreduktionsreaktionskatalysatorer
- Ingen festivaler, ingen skoleelever:Unge går glip af vitale overgangsritualer under COVID
- Damptrykket af en prøve kogende vand er 380 torr temperatur er det?
- Forældrekontrol forhindrer ikke teenagere i at se pornografi, nye forskningsfund
- Gamma-stråleteleskoper afslører en højenergifælde i vores galaksecenter
- Hvordan kan kromatografi bruges til at vise, at hydrolysen af stivelse kun producerer ét sukker?


