Kvantetal for magnesiumvalenselektroner:en trin-for-trin guide
1. Elektronisk konfiguration:
* Magnesium (Mg) har et atomnummer på 12, hvilket betyder, at det har 12 elektroner.
* Dens elektroniske konfiguration er 1s² 2s² 2p⁶ 3s².
2. Identifikation af valenselektroner:
* Valenselektroner er elektronerne i det yderste energiniveau. For magnesium er det de to elektroner i 3s orbitalen.
3. Kvantetal:
* n (Principal Quantum Number): Dette beskriver energiniveauet. For 3s elektronerne er n =3.
* l (azimuttal eller vinkelmoment kvantetal): Dette beskriver formen af orbitalen. For en s orbital er l =0.
* ml (magnetisk kvantetal): Dette beskriver orbitalens orientering i rummet. For en s orbital er der kun én orientering, så ml =0.
* ms (Spin Quantum Number): Dette beskriver elektronens iboende vinkelmomentum, som også kaldes spin. Elektroner har et spin på enten +1/2 eller -1/2. Da vi har to elektroner i 3s orbitalen, vil den ene have ms =+1/2 og den anden vil have ms =-1/2.
Derfor er et muligt sæt kvantetal for en af valenselektronerne i et magnesiumatom i grundtilstand:
*n =3
* l =0
*ml =0
* ms =+1/2 (eller ms =-1/2)
Sidste artikelBond Order:Styrken af kemiske bindinger forklaret
Næste artikelEthanolforbrænding:Produkter og kemisk reaktion forklaret
 Varme artikler
Varme artikler
-
 Forståelse af aktiveringsenergi i jod-urreaktionenAf Jack Brubaker, opdateret 30. august 2022 Billedkredit:Apiwan Borrikonratchata/iStock/GettyImages Jod-ur-reaktionen er en klassisk demonstration, der bruges af gymnasieelever og kemistuderende til
Forståelse af aktiveringsenergi i jod-urreaktionenAf Jack Brubaker, opdateret 30. august 2022 Billedkredit:Apiwan Borrikonratchata/iStock/GettyImages Jod-ur-reaktionen er en klassisk demonstration, der bruges af gymnasieelever og kemistuderende til -
 Ren teknologi til fremstilling af lavmolekylær chitosanPlasma-assisteret depolymerisation af chitosan i en kvartsblandingsanordning. Kredit:MIPT Forskere ved MIPT har udviklet en ny teknik til at opnå lavmolekylær vægt, vandopløseligt kitin og chitosa
Ren teknologi til fremstilling af lavmolekylær chitosanPlasma-assisteret depolymerisation af chitosan i en kvartsblandingsanordning. Kredit:MIPT Forskere ved MIPT har udviklet en ny teknik til at opnå lavmolekylær vægt, vandopløseligt kitin og chitosa -
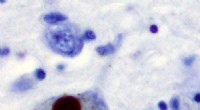 Ubrugeligt Parkinsons-molekyle spilder sine hemmelighederImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere fra UC San Francisco har for
Ubrugeligt Parkinsons-molekyle spilder sine hemmelighederImmunhistokemi for alfa-synuclein, der viser positiv farvning (brun) af et intraneuralt Lewy-legeme i Substantia nigra ved Parkinsons sygdom. Kredit:Wikipedia Forskere fra UC San Francisco har for -
 Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne
Forskere udvikler 3D-trykte biomaterialer, der nedbrydes efter behovBrune forskere har fundet en måde at 3D-udskrive indviklede midlertidige mikrostrukturer, der kan nedbrydes efter behov ved hjælp af en biokompatibel kemisk trigger. Teknikken kunne være nyttig kunne
- Forskere måler kvanteegenskaber af nanorør, afgørende for næste generations elektronik
- Er det at se tro? Ved udbredelse af politik er videoer måske ikke meget mere overbevisende end dere…
- Nokia melder om højere overskud, øger 5G-investeringer
- Depolarisering og repolarisering af cellemembranen <p> <p> Nerveceller i hvile har en elektrisk ladn…
- Fra koraller til afgrøder:Hvordan livet beskytter planerne for dets cellulære kraftværker
- Pas på de videnskabelige undersøgelser - de fleste tager fejl, forsker advarer


