Carbotermisk reduktion:Metaller renset ved opvarmning med kulstof
Kemien:
* Kulstof er et godt reduktionsmiddel. Det afgiver let elektroner og bliver oxideret (taber elektroner).
* Metaloxider i malme er typisk i +2 eller +3 oxidationstilstand, hvilket betyder, at de har en positiv ladning.
* Når opvarmet med kulstof , reducerer kulstoffet metaloxidet. Kulstoffet tager ilten og danner kuldioxid (CO2), mens metallet efterlades i sin elementære form.
Eksempler:
Her er nogle eksempler på metaller, der kan renses ved hjælp af denne metode:
* Jern (Fe): Jernmalm (Fe2O3) opvarmes med koks (en form for kulstof) i en højovn for at fremstille jern.
* Zink (Zn): Zinkoxid (ZnO) opvarmes med kulstof for at producere zink.
* Tin (Sn): Tinoxid (SnO2) opvarmes med kulstof til fremstilling af tin.
* Lead (Pb): Blyoxid (PbO) opvarmes med kulstof for at producere bly.
Vigtige overvejelser:
* Reaktivitet: Metaller, der er mere reaktive end kulstof, kan ikke reduceres ved denne metode. For eksempel er natrium (Na) og kalium (K) mere reaktive end kulstof og kræver forskellige metoder til oprensning.
* Temperatur: Den temperatur, der kræves for at reaktionen kan finde sted, varierer afhængigt af metallet. Nogle reaktioner kræver meget høje temperaturer, mens andre sker ved lavere temperaturer.
Oversigt:
Den carbotermiske reduktionsmetode er en enkel og effektiv måde at rense metaller, der er mindre reaktive end kulstof. Det er meget brugt i industrien til at producere forskellige metaller.
 Varme artikler
Varme artikler
-
 En metode til at genvinde skjulte serienumre fra polymerprodukterGendannelse af slettede serienumre i en polymer. Kredit:American Chemical Society Polymerer er meget udbredt i industrien og anvendes i stigende grad som erstatninger for metaller ved fremstilling
En metode til at genvinde skjulte serienumre fra polymerprodukterGendannelse af slettede serienumre i en polymer. Kredit:American Chemical Society Polymerer er meget udbredt i industrien og anvendes i stigende grad som erstatninger for metaller ved fremstilling -
 Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br
Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br -
 Malaria kan fældes af en antarktisk havsvampAntarktis havsvampekstrakter giver bly til nye malariabehandlinger. Kredit:Bill Baker Det kolde vand i Antarktis kan give behandling for en dødelig sygdom, der påvirker befolkningen på nogle af de
Malaria kan fældes af en antarktisk havsvampAntarktis havsvampekstrakter giver bly til nye malariabehandlinger. Kredit:Bill Baker Det kolde vand i Antarktis kan give behandling for en dødelig sygdom, der påvirker befolkningen på nogle af de -
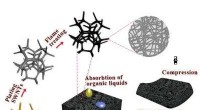 Fremstillingsmetode i stor skala med SWNT -svampe af høj kvalitet3D carbon nanorørsvampen fremstillet ved superhurtig flammebrændingsmetode. Kredit:Shihong Yue I et papir udgivet i Nano , en gruppe forskere rapporterer om at udvikle en simpel flammebrændingsm
Fremstillingsmetode i stor skala med SWNT -svampe af høj kvalitet3D carbon nanorørsvampen fremstillet ved superhurtig flammebrændingsmetode. Kredit:Shihong Yue I et papir udgivet i Nano , en gruppe forskere rapporterer om at udvikle en simpel flammebrændingsm
- Hvilken type overfladegrund findes ofte i New York State mellem Elmira og Ithaca?
- Hvilken form for energi er ikke forbundet med partikler et objekt?
- Opbygning af mere fleksible barrierer for at redde liv på landevejene
- Befolkning er kun en del af historien om tornadoskader
- Når MSNBC eller Fox News sendes på offentlige steder, hvordan reagerer folk?
- Nu ser du det, nu gør du det ikke:Skjulte farver opdaget ved et tilfælde


