Forståelse af ilts elektronegativitet i vandmolekyler
Her er en oversigt:
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner mod sig selv, når det danner en kemisk binding.
* Oxygens elektronegativitet: Ilt har en elektronegativitetsværdi på 3,44 på Pauling-skalaen.
* Brints elektronegativitet: Brint har en elektronegativitetsværdi på 2,20 på Pauling-skalaen.
Forskellen gør en forskel:
Den større elektronegativitetsforskel mellem oxygen og brint betyder, at oxygen tiltrækker de delte elektroner i O-H-bindingerne stærkere. Dette fører til:
* Polære kovalente bindinger: Den ulige deling af elektroner skaber delvise positive ladninger på brintatomerne (δ+) og en delvis negativ ladning på oxygenatomet (δ-).
* Et polært molekyle: Det overordnede molekyle har et dipolmoment, hvor den ene ende er svagt negativ og den anden let positiv. Denne polaritet er afgørende for vands unikke egenskaber, som dets evne til at opløse mange stoffer og fungere som opløsningsmiddel.
Opsummering:
Ilts større elektronegativitet er den grundlæggende årsag til, at det trækker elektroner mod sig selv i vandmolekyler, hvilket skaber den karakteristiske polære struktur, der styrer mange af vands egenskaber.
 Varme artikler
Varme artikler
-
 En praktisk guide til de seks kernetyper af kemiske reaktionerAf Lan Luo Opdateret 30. august 2022 Jardul/iStock/GettyImages Kemiske reaktioner er en integreret del af moderne teknologi og hverdagsliv – fra at drive motorer til at brygge drikkevarer. De drive
En praktisk guide til de seks kernetyper af kemiske reaktionerAf Lan Luo Opdateret 30. august 2022 Jardul/iStock/GettyImages Kemiske reaktioner er en integreret del af moderne teknologi og hverdagsliv – fra at drive motorer til at brygge drikkevarer. De drive -
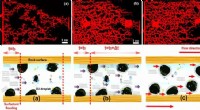 En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati -
 Hårde magnetiske belægninger til højpræcisionsmikroskopiMikroskopplade med magnetisk positionering. Kredit:ITK Dr. Kassen GmbH Mikroskopi er i spidsen for kampen mod coronavirus. Specielle mikroskoper, som gør det muligt for forskere at se små cellestr
Hårde magnetiske belægninger til højpræcisionsmikroskopiMikroskopplade med magnetisk positionering. Kredit:ITK Dr. Kassen GmbH Mikroskopi er i spidsen for kampen mod coronavirus. Specielle mikroskoper, som gør det muligt for forskere at se små cellestr -
 Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli
Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli
- Hvad er faretegn på sur regn?
- NASA, ATLAS til moden bærbar rumkommunikationsteknologi
- Californien vil sandsynligvis ikke opfylde skelsættende mål for reduktion af drivhusgasemissioner
- Hvilken videnskabsmand opdagede, at solen er stationær og jord bevæger sig?
- Studiet løser mysteriet om, hvordan de første dyr opstod på Jorden
- Hvad betyder ordet tyngdekraft i videnskaben?


