Ammoniumnitrat:Polaritet forklaret - kemiske egenskaber og struktur
* Molekylær form: Ammoniumionen (NH4⁺) har en tetraedrisk form, mens nitrationen (NO3⁻) har en trigonal plan form. Dette arrangement af atomer fører til en ujævn fordeling af elektrontæthed.
* Elektronegativitetsforskel: Nitrogen- og oxygenatomerne i begge ioner har betydeligt højere elektronegativitet end hydrogen. Det betyder, at de trækker elektrontæthed mod sig selv, hvilket skaber partielle negative ladninger (δ-) på nitrogen- og oxygenatomerne og partielle positive ladninger (δ+) på brintatomerne.
* Dipolmoment: Den ujævne fordeling af ladninger resulterer i et netto dipolmoment for begge ioner. Da ammonium- og nitrationerne har modsatte ladninger, justeres deres dipoler, hvilket bidrager til ammoniumnitratmolekylets samlede polaritet.
Opsummering: Ammoniumnitrat er et polært molekyle på grund af den ujævne fordeling af elektrontæthed på grund af elektronegativitetsforskellen mellem atomerne og det samlede dipolmoment skabt af de individuelle ioner.
Sidste artikelBeregn oxidationstallet for nitrogen i N₂O₅:En trin-for-trin guide
Næste artikelLiOH + H2O-reaktion:Forstå opløsningsprocessen
 Varme artikler
Varme artikler
-
 For CRISPR, justering af DNA-fragmenter før indsættelse giver de højeste effektivitetsrater endnuProfessor Huimin Zhao ledede et team, der opnåede den højeste rapporterede effektivitet ved at indsætte gener i humane celler med CRISPR-Cas9. Kredit:L. Brian Stauffer Forskere fra University of I
For CRISPR, justering af DNA-fragmenter før indsættelse giver de højeste effektivitetsrater endnuProfessor Huimin Zhao ledede et team, der opnåede den højeste rapporterede effektivitet ved at indsætte gener i humane celler med CRISPR-Cas9. Kredit:L. Brian Stauffer Forskere fra University of I -
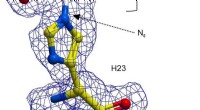 Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere
Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere -
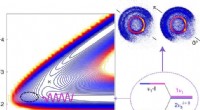 Brug af kvantevibrationsegenskaber mellem molekyler til at fremskynde reaktioner mellem forbindelserGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00914-3 Et par forskere, den ene med Southern University of Science and Technology, den anden Institute of Atomic and Molecu
Brug af kvantevibrationsegenskaber mellem molekyler til at fremskynde reaktioner mellem forbindelserGrafisk abstrakt. Kredit:Nature Chemistry (2022). DOI:10.1038/s41557-022-00914-3 Et par forskere, den ene med Southern University of Science and Technology, den anden Institute of Atomic and Molecu -
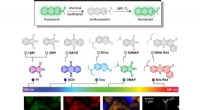 Et-atoms switch overlader fluorescerende farvestofferØverst, en sekvens viser designet af thio-caged farvestoffer designet på Rice University til at blive udløst af synligt lys. I bunden, konfokal og superopløsningsbilleddannelse af en lipiddråbe i leve
Et-atoms switch overlader fluorescerende farvestofferØverst, en sekvens viser designet af thio-caged farvestoffer designet på Rice University til at blive udløst af synligt lys. I bunden, konfokal og superopløsningsbilleddannelse af en lipiddråbe i leve
- Detektering af dopamin i femtomolære koncentrationer
- Snapchat lancerer egen multi-player gaming platform
- Hvad er den vigtigste faktor, der kontrollerer udviklingen af en stjerne, og hvorfor?
- Hvad er en syntesereaktion?
- Skyldes forhøjede niveauer af kviksølv i den amerikanske dyppe afløbsdæmninger?
- Kæmpe Puerto Rico-radioteleskop, der lukker i slag for videnskaben


