Beregn pH-værdien af en salpetersyreopløsning:en trin-for-trin guide
1. Beregn molariteten af salpetersyreopløsningen:
* Molar masse af HNO₃: 1 (H) + 14 (N) + 3 * 16 (O) =63 g/mol
* Moler HNO₃: 12,6 g / 63 g/mol =0,2 mol
* Molaritet (M): 0,2 mol / 0,250 L =0,8 M
2. Salpetersyre er en stærk syre, så den ioniseres fuldstændigt i opløsning:
HNO3 (aq) → H+ (aq) + NO3⁻ (aq)
Dette betyder, at koncentrationen af H⁺-ioner er lig med koncentrationen af salpetersyreopløsningen.
3. Beregn pH:
* pH =-log[H⁺]
* pH =-log(0,8)
* pH ≈ 0,1
Derfor er pH-værdien af den 250,0 ml vandige opløsning indeholdende 12,6 g salpetersyre ca. 0,1.
 Varme artikler
Varme artikler
-
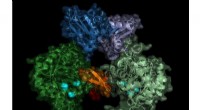 Forskerhold finder mulig ny tilgang til sovesygemedicinStruktur af parasittens IMP-dehydrogenase. Det aktive enzym danner par (dimerer), switch-området (Bateman-regionen) vises i blå nuancer. Kredit:Lübeck Universitet/DESY, Lars Redecke Ved hjælp af u
Forskerhold finder mulig ny tilgang til sovesygemedicinStruktur af parasittens IMP-dehydrogenase. Det aktive enzym danner par (dimerer), switch-området (Bateman-regionen) vises i blå nuancer. Kredit:Lübeck Universitet/DESY, Lars Redecke Ved hjælp af u -
 Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr.
Fremstilling af metal-organiske ramme-baserede kompositter for effektivitetKandidatstuderende Yufeng Quan og Ruiqing Shen bruger en dobbeltskrueekstruder i bænkskala til bæredygtig og effektiv fremstilling af metal-organiske ramme-baserede polymer nanokompositter. Kredit:Dr. -
 Grafenkortlægning 50 gange hurtigereDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Grafen har skabt høje forventninger, som en stærk, ultra tynd, todimensionelt materiale, der også
Grafenkortlægning 50 gange hurtigereDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Grafen har skabt høje forventninger, som en stærk, ultra tynd, todimensionelt materiale, der også -
 Lagring af data som blandinger af fluorescerende farvestofferBlandinger af fluorescerende farvestofmolekyler, placeret små steder på en epoxyoverflade med en inkjetprinter, kode data. Kredit:American Chemical Society. Efterhånden som verdens behov for datal
Lagring af data som blandinger af fluorescerende farvestofferBlandinger af fluorescerende farvestofmolekyler, placeret små steder på en epoxyoverflade med en inkjetprinter, kode data. Kredit:American Chemical Society. Efterhånden som verdens behov for datal
- Hvad er de to hovedtype af terræn på månen?
- Kan man producere energi med en bi-metalstrimmel, når den opvarmes?
- Hvad hedder Compound BII3?
- Er der en mandlig forsørgernorm? Se ikke på ægtefællers indkomst for at finde ud af, siger under…
- Hvor er den kontinentale skorpe?
- Bare et lille stykke papir kan gøre vandforbruget mere sikkert


