Dobbelt kulstof-kulstofbindinger:egenskaber, dannelse og eksempler
Her er en oversigt:
* Kovalent binding: En binding dannet ved deling af elektroner mellem atomer.
* Dobbeltbinding: En binding, hvor to par elektroner er delt.
* Carbon-carbon-binding: En binding specifikt mellem to carbonatomer.
Karakteristika for en dobbelt carbon-carbon-binding:
* Stærkere: Delingen af to elektronpar skaber en stærkere tiltrækning mellem kulstofatomerne, hvilket gør bindingen sværere at bryde.
* Kortere: Den øgede elektrontæthed mellem carbonatomerne trækker dem tættere sammen, hvilket resulterer i en kortere bindingslængde.
* Plan geometri: Dobbeltbindingen tvinger de atomer, der er forbundet med carbonerne, til at ligge i samme plan.
* Begrænset rotation: Dobbeltbindingen forhindrer fri rotation omkring bindingsaksen.
Eksempler på molekyler, der indeholder dobbelte carbon-carbon-bindinger:
* Ethylen (C2H4): Det enkleste molekyle, der indeholder en dobbeltbinding.
* Benzen (C6H6): Indeholder skiftende enkelt- og dobbeltbindinger i en ringstruktur.
* Alkener: En klasse af carbonhydrider med mindst én carbon-carbon dobbeltbinding.
Betydningen af dobbelte carbon-carbon-bindinger:
* Reaktivitet: Dobbeltbindinger er mere reaktive end enkeltbindinger på grund af tilstedeværelsen af elektroner i pi-bindingen. Dette giver mulighed for forskellige kemiske reaktioner som tilsætning og oxidation.
* Struktur og funktion: Dobbeltbindinger spiller en afgørende rolle i strukturen og funktionen af mange organiske molekyler, herunder proteiner, lipider og kulhydrater.
* Industrielle applikationer: Dobbeltbindinger bruges til fremstilling af plast, syntetiske fibre og andre industrielle materialer.
Sammenfattende er en dobbelt carbon-carbon-binding et centralt strukturelt træk i organisk kemi, hvilket bidrager til mange molekylers unikke egenskaber og reaktivitet.
Sidste artikelKemisk vs. fysisk ændring i madlavning:Forstå forskellen
Næste artikelCalciumchlorid og saltsyrereaktion:Hvad sker der?
 Varme artikler
Varme artikler
-
 Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s
Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s -
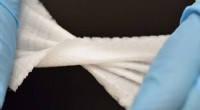 3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh
3D-trykt Biomesh minimerer brokreparationskomplikationer3D -printet Biomesh demonstrerer sin mekaniske styrke og fleksibilitet. Kredit:Baylor College of Medicine Brok er en af de mest almindelige bløde vævsskader. Brok dannes ved intra-abdominal indh -
 Forskere i verden afslører først strukturen af et vigtigt lægemiddelmålKredit:Monash University Monash University-forskere har brugt en ny teknik til at afsløre strukturen af et vigtigt lægemiddelmål, åbner vejen for forbedrede behandlinger af kroniske sygdomme som
Forskere i verden afslører først strukturen af et vigtigt lægemiddelmålKredit:Monash University Monash University-forskere har brugt en ny teknik til at afsløre strukturen af et vigtigt lægemiddelmål, åbner vejen for forbedrede behandlinger af kroniske sygdomme som -
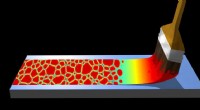 Beregning af den bedste fremstillingsstrategi for organiske elektroniske komponenterVed hjælp af computersimuleringer, MPI-P-forskere kan forudsige strukturen af krystaller i organiske halvlederlag. Kredit:Max Planck Society Halvledere lavet af organiske materialer, f.eks. til
Beregning af den bedste fremstillingsstrategi for organiske elektroniske komponenterVed hjælp af computersimuleringer, MPI-P-forskere kan forudsige strukturen af krystaller i organiske halvlederlag. Kredit:Max Planck Society Halvledere lavet af organiske materialer, f.eks. til
- Ny probe for stofskiftesygdomme
- At behandle ikke-mennesker som interessenter er nøglen til bæredygtige teknologier
- Hvilken type bølge rejser mediet i en cirkulær bevægelse?
- Konform meta -overfladebelægning eliminerer krydstale og krymper bølgeledere
- Hvilken type erosion dannede sandklitter?
- Hvad bruger videnskabsmand til at måle energiindholdet i fødevarer?


