Sulfation (SO₄²⁻):Form, bindingsvinkel og struktur forklaret
Her er hvorfor:
* Centralt atom: Det centrale atom er svovl (S).
* Omgivende atomer: Fire oxygen (O) atomer er bundet til svovlatomet.
* Elektronpar: Svovl har seks valenselektroner, og hvert oxygenatom bidrager med en elektron til at danne en kovalent binding. Dette giver i alt 12 valenselektroner. Disse elektroner er arrangeret i fire bindingspar og to ensomme par omkring svovlatomet.
* VSEPR-teori: De fire bindingspar og to enlige par omkring svovl resulterer i en tetraedrisk elektrongeometri. Frastødningen mellem elektronparrene skubber bindingsparrene tættere sammen, hvilket fører til en lidt mindre bindingsvinkel end den ideelle 109,5°.
Visuel repræsentation:
Du kan visualisere dette ved at forestille dig en pyramide med fire flader og et svovlatom i midten. De fire iltatomer optager de fire hjørner af pyramiden.
 Varme artikler
Varme artikler
-
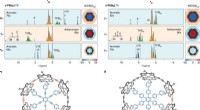 Største rekord for aromatisk ringstørrelse brudt med 162 π elektronerH NMR-spektre af de aromatiske og antiaromatiske seks-porphyrin nanoreringsskabelonkomplekser i oxidationstilstande 2+, 4+ og 6+. Kredit: Naturkemi (2020). DOI:10.1038/s41557-019-0398-3 Et team
Største rekord for aromatisk ringstørrelse brudt med 162 π elektronerH NMR-spektre af de aromatiske og antiaromatiske seks-porphyrin nanoreringsskabelonkomplekser i oxidationstilstande 2+, 4+ og 6+. Kredit: Naturkemi (2020). DOI:10.1038/s41557-019-0398-3 Et team -
 Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ
Kobberoxidfotokatoder:Lasereksperiment afslører placeringen af effektivitetstabEn grøn laserimpuls exciterer indledningsvis elektronerne i Cu2O; kun brøkdele af et sekund senere, en anden laserimpuls (UV-lys) sonderer energien af den exciterede elektron. Kredit:M. Kuensting/HZ -
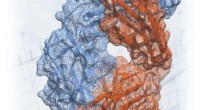 At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de
At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de -
 Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin
Forskere til at skabe galaktiske byggesten til at studere rummet mellem stjernerForskere planlægger at syntetisere en klasse af kemiske forbindelser for at afgøre, om de er en vigtig byggesten til fremstilling af galakser. Holdet fra Imperial College London har modtaget startfin
- Efter et skandalefyldt år, hvad er det næste for Facebook?
- Ville gasafgiftslettelser gøre en stor forskel, når priserne skyder i vejret? Vi spurgte 4 ekspert…
- Ujævne flydende film kunne forenkle fremstillingen af mikrolinser
- Ny røntgenmikroskopiteknik afslører nanoskala hemmeligheder bag genopladelige batterier
- Ti forslag til kvindelige undervisere og ansatte under pandemien
- Når du opvarmer en gryde over flamme, hvilken form for energi tilsættes til vandet?


