Beregning af aluminiumoxidproduktion:En støkiometriguide
* Hvad er den anden reaktant? Aluminiumoxid dannes ved en reaktion mellem aluminium og ilt. Du skal vide, hvor meget ilt der er til stede for at bestemme mængden af produceret aluminiumoxid.
* Hvad er reaktionsligningen? At kende den afbalancerede kemiske ligning vil give os mulighed for at beregne støkiometrien af reaktionen.
For eksempel:
Hvis reaktionen er:
4 Al + 3 O2 → 2 Al203
Og du har 6,4 gram aluminium (Al) , kan vi følge disse trin:
1. Konverter gram aluminium til mol:
- Find den molære masse af aluminium (Al):26,98 g/mol
- Divider massen af aluminium med dets molære masse:6,4 g / 26,98 g/mol =0,237 mol Al
2. Brug molforholdet fra den balancerede ligning:
- Ligningen viser, at 4 mol Al reagerer og danner 2 mol Al₂O3.
- Molforholdet er 4:2 eller 2:1 (forenklet).
- Derfor vil 0,237 mol Al producere 0,237 mol / 2 =0,119 mol Al2O3.
3. Konverter mol aluminiumoxid til gram:
- Find den molære masse af aluminiumoxid (Al₂O₃):101,96 g/mol
- Multiplicer mol Al2O3 med dens molære masse:0,119 mol * 101,96 g/mol =12,17 gram Al₂O₃
Angiv venligst de manglende oplysninger, så jeg kan give dig det rigtige svar.
 Varme artikler
Varme artikler
-
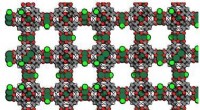 Tamning af defekte porøse materialer til robust og selektiv heterogen katalyseRepræsentation af (Ru) HKUST-1 MOF. Kredit:Manuel A. Ortuño Produktionen af 1-buten via ethylen-dimerisering er en af de få industrielle processer, der anvender homogen katalyse på grund af de
Tamning af defekte porøse materialer til robust og selektiv heterogen katalyseRepræsentation af (Ru) HKUST-1 MOF. Kredit:Manuel A. Ortuño Produktionen af 1-buten via ethylen-dimerisering er en af de få industrielle processer, der anvender homogen katalyse på grund af de -
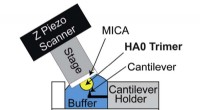 Virulensfaktor for influenza A-virus kortlagt i realtidHS-AFM opsætning til direkte visualisering af HA0 trimer. Skematisk diagram over HS-AFM-opsætningen til scanning af HA0-trimeren. Kredit:Kanazawa University Influenza A -vira, som tidligere er ans
Virulensfaktor for influenza A-virus kortlagt i realtidHS-AFM opsætning til direkte visualisering af HA0 trimer. Skematisk diagram over HS-AFM-opsætningen til scanning af HA0-trimeren. Kredit:Kanazawa University Influenza A -vira, som tidligere er ans -
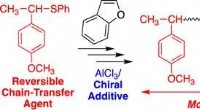 Oprettelse af mere miljøvenlig, varmebestandig og gennemsigtig plastGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.2c02569 Forskere i Japan har udviklet en ny teknik til at skabe polymerer. Denne opdagelse forventes at fø
Oprettelse af mere miljøvenlig, varmebestandig og gennemsigtig plastGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.2c02569 Forskere i Japan har udviklet en ny teknik til at skabe polymerer. Denne opdagelse forventes at fø -
 Forskere i verden afslører først strukturen af et vigtigt lægemiddelmålKredit:Monash University Monash University-forskere har brugt en ny teknik til at afsløre strukturen af et vigtigt lægemiddelmål, åbner vejen for forbedrede behandlinger af kroniske sygdomme som
Forskere i verden afslører først strukturen af et vigtigt lægemiddelmålKredit:Monash University Monash University-forskere har brugt en ny teknik til at afsløre strukturen af et vigtigt lægemiddelmål, åbner vejen for forbedrede behandlinger af kroniske sygdomme som
- Hvad er den molekylære formel på 284,77G Mol CCL?
- Hvilke energitransformationer af et stearinlys brænder?
- Carboxylsyrer er moderat stærkere end 2-naphthol?
- Hvad tror du, der vil ske med en dyrecelle, hvis dens membran brister, ville det samme som en plante…
- Video viser en beskadiget rørledning, der er ansvarlig for olieudslip ud for Orange Countys kyst
- Hvor mange centimeter er tre og halvdelen?


