Stærke elektrolytter, syrer og baser:Forståelse af sammenhængen
* Stærke elektrolytter: Det er stoffer, der fuldstændigt ioniserer (brækkes fra hinanden til ioner), når de opløses i vand. Det betyder, at de producerer en høj koncentration af ioner i opløsning, hvilket gør dem til fremragende ledere af elektricitet.
* Stærke syrer: Det er syrer, der fuldstændigt ioniserer i vand og frigiver en høj koncentration af hydrogenioner (H+). Da de ioniserer fuldstændigt, er de også stærke elektrolytter.
* Stærke baser: Disse er baser, der fuldstændigt ioniserer i vand og frigiver en høj koncentration af hydroxidioner (OH-). Ligesom stærke syrer er de stærke elektrolytter på grund af deres fuldstændige ionisering.
Nøglepunkter:
* Ikke alle stærke elektrolytter er syrer eller baser: For eksempel er salte som natriumchlorid (NaCl) stærke elektrolytter, men de er hverken sure eller basiske.
* Ikke alle syrer og baser er stærke: Svage syrer og svage baser ioniseres kun delvist i vand, hvilket betyder, at de ikke er stærke elektrolytter.
Eksempler:
* Stærk syre og stærk elektrolyt: Saltsyre (HCl) ioniseres fuldstændigt til H+ og Cl-ioner i vand.
* Stærk base og stærk elektrolyt: Natriumhydroxid (NaOH) ioniseres fuldstændigt til Na+ og OH- ioner i vand.
* Svag syre og svag elektrolyt: Eddikesyre (CH3COOH) ioniserer kun delvist i vand, hvilket giver en lavere koncentration af H+ ioner sammenlignet med en stærk syre.
Opsummering:
* Stærke syrer og stærke baser er undergrupper af stærke elektrolytter. De er stærke elektrolytter, fordi de ioniserer fuldstændigt.
* Det er dog ikke alle stærke elektrolytter, der er stærke syrer eller baser.
Sidste artikelHBr:Stærk syre eller base? Forståelse af surhed
Næste artikelKOH:Stærke baseegenskaber og dissociation forklaret
 Varme artikler
Varme artikler
-
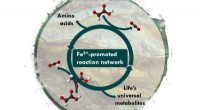 Lifes biokemiske netværk kunne have dannet sig spontant på JordenSyntese og nedbrydning af universelle metaboliske forstadier fremmet af jern Kredit:University of Strasbourg Forskere i Strasbourg, Frankrig, har fundet ud af at blande to små biomolekyler, glyoxy
Lifes biokemiske netværk kunne have dannet sig spontant på JordenSyntese og nedbrydning af universelle metaboliske forstadier fremmet af jern Kredit:University of Strasbourg Forskere i Strasbourg, Frankrig, har fundet ud af at blande to små biomolekyler, glyoxy -
 Sådan bestemmes neutroner, protoner og elektroner i atomer, ioner og isotoperAf Riti Gupta – Opdateret 24. marts 2022 Når du skal identificere den subatomære sammensætning af enhver kemisk art, er det periodiske system din primære reference. Nedenfor er en klar guide til, hvo
Sådan bestemmes neutroner, protoner og elektroner i atomer, ioner og isotoperAf Riti Gupta – Opdateret 24. marts 2022 Når du skal identificere den subatomære sammensætning af enhver kemisk art, er det periodiske system din primære reference. Nedenfor er en klar guide til, hvo -
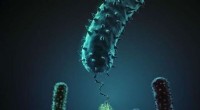 Bakteriel adhæsion in vitro og in silicoDenne figur viser, hvordan stafylokokker adhæsionsprotein (i grønt) interagerer med dets beslægtede peptidligand (rød). Kredit:H. Gaub, LMU München Ludwig-Maximilians-Universitaet (LMU) forskere
Bakteriel adhæsion in vitro og in silicoDenne figur viser, hvordan stafylokokker adhæsionsprotein (i grønt) interagerer med dets beslægtede peptidligand (rød). Kredit:H. Gaub, LMU München Ludwig-Maximilians-Universitaet (LMU) forskere -
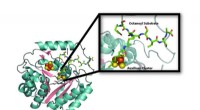 Vedvarende ressource:For at producere vital liponsyre, svovl bruges, derefter genopfyldesModel af krystalstrukturen af lipoylsyntaseenzymet (LipA) fra bakterierne Mycobacterium tuberculosis, der afslører ødelæggelsen af en af dens jern-svovlklynger (orange og gule kugler) til brug s
Vedvarende ressource:For at producere vital liponsyre, svovl bruges, derefter genopfyldesModel af krystalstrukturen af lipoylsyntaseenzymet (LipA) fra bakterierne Mycobacterium tuberculosis, der afslører ødelæggelsen af en af dens jern-svovlklynger (orange og gule kugler) til brug s
- Hvad er 3 undersøgelsesmetoder inden for videnskab?
- Hvad bruges væsken til at plette prøver på et mikroskop?
- Hvilken type celledeling forekommer i alle celler et organismelegeme undtagen reproduktive celler?
- Ny start Zapata Computing har til hensigt at markedsføre kvantecomputersoftware
- Hvad får du, når du kemisk kombinerer klorgas og natrium?
- Forskere udfører forskning for bedre at forstå, hvorfor unge voksne vælger at flytte til det land…


