Ionisk ledningsevne og ionstørrelse:En detaljeret forklaring
1. Mobilitet:
* Mindre ioner er generelt mere mobile: Mindre ioner oplever mindre friktion med de omgivende opløsningsmiddelmolekyler eller krystalgitter. Dette giver dem mulighed for at bevæge sig lettere gennem mediet, hvilket øger ledningsevnen.
* Større ioner oplever større modstand: Større ioner har et større overfladeareal, hvilket fører til større interaktion med det omgivende miljø, hvilket øger modstanden og reducerer mobiliteten.
2. Hydrering:
* Mindre ioner har højere hydreringstal: De har en højere ladningstæthed, tiltrækker flere opløsningsmiddelmolekyler (som vand) og danner en hydreringsskal omkring dem. Denne skal øger ionens effektive størrelse, hvilket hindrer dens bevægelse.
* Større ioner har lavere hydreringstal: De har lavere ladningstæthed, hvilket tiltrækker færre opløsningsmiddelmolekyler. Dette fører til en mindre hydreringsskal og potentielt større mobilitet.
* Dette er dog ikke altid tilfældet: Hydratiseringstallet kan være væsentligt påvirket af ladningen på ionen, og nogle gange kan større ioner have højere hydratiseringstal.
3. Gitterstruktur (i faste stoffer):
* Mindre ioner passer bedre i krystalgitteret: I ioniske faste stoffer kan mindre ioner lettere optage rum i krystalgitteret. Dette giver mulighed for større ionmigrering og øget ledningsevne.
* Større ioner forstyrrer gitteret: Store ioner kan forstyrre den regelmæssige struktur af gitteret, hvilket fører til lavere ledningsevne.
4. Koncentration:
* Høj koncentration kan reducere ledningsevnen: Selvom det virker kontraintuitivt, kan ioner ved høje koncentrationer forstyrre hinandens bevægelser, hvilket reducerer den samlede ledningsevne. Dette skyldes øgede ion-ion-interaktioner.
5. Temperatur:
* Øget temperatur forbedrer generelt ledningsevnen: Ved højere temperaturer har ionerne mere kinetisk energi, hvilket giver dem mulighed for at bevæge sig mere frit og overvinde barriererne for deres bevægelse.
Opsummering:
Mens en mindre størrelse generelt oversætter til højere mobilitet og bedre ionisk ledningsevne, er ionstørrelsens indflydelse på ledningsevnen ikke ligetil. Det er et komplekst samspil mellem flere faktorer, herunder hydrering, gitterstruktur, koncentration og temperatur.
Eksempler:
* Lithium-ion-batterier: Lithium-ioner er små og meget mobile, hvilket gør dem ideelle til brug i batterier.
* Natrium-ion-batterier: Natriumioner er større end lithiumioner, men de er stadig relativt mobile og kan bruges i batterier.
* Magnesium-ion-batterier: Magnesiumioner er endnu større end natriumioner, hvilket gør dem mindre mobile og fører til lavere ledningsevne.
Derfor er det afgørende at overveje alle disse faktorer, når man designer materialer til specifikke applikationer, der er afhængige af ionisk ledningsevne.
 Varme artikler
Varme artikler
-
 Ny 3D-udskrivningsmetode kan transformere materiale bag vital medicinsk isotopLaboratoriets nye 3D-udskrivningstilgang gør sin genbrugsmetode-banebrydende i 2015 af Mo-99-programchef Peter Tkac (til venstre) og andre-hurtigere, mere pålidelig, og mere omkostningseffektivt. Også
Ny 3D-udskrivningsmetode kan transformere materiale bag vital medicinsk isotopLaboratoriets nye 3D-udskrivningstilgang gør sin genbrugsmetode-banebrydende i 2015 af Mo-99-programchef Peter Tkac (til venstre) og andre-hurtigere, mere pålidelig, og mere omkostningseffektivt. Også -
 Ny måde at opdage ekstase påKredit:Syddansk Universitet Mens man bygger molekylære maskiner, forskere faldt over en ny metode til at opdage ekstase. Opdagelsen kan føre til mere pålidelige lægemiddeltest. Forskere ved Sydda
Ny måde at opdage ekstase påKredit:Syddansk Universitet Mens man bygger molekylære maskiner, forskere faldt over en ny metode til at opdage ekstase. Opdagelsen kan føre til mere pålidelige lægemiddeltest. Forskere ved Sydda -
 Ny forskning identificerer Fukushima -reaktormateriale i miljøetEt 3D-billede, der tillod forskerne at opdage fordelingen af elementer i prøven. Kredit:University of Bristol/Diamond Light Source Gennem analyse af specifikke nedfaldspartikler i miljøet, et fæ
Ny forskning identificerer Fukushima -reaktormateriale i miljøetEt 3D-billede, der tillod forskerne at opdage fordelingen af elementer i prøven. Kredit:University of Bristol/Diamond Light Source Gennem analyse af specifikke nedfaldspartikler i miljøet, et fæ -
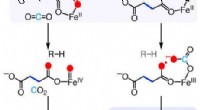 Vejen til fremstilling af ethylenMekanismer for de ethylen-dannende enzym (EFE) reaktioner. Ny forskning beskriver de kemiske trin, som dette naturligt forekommende enzym bruger til at omdanne en almindelig kemisk forbindelse til eth
Vejen til fremstilling af ethylenMekanismer for de ethylen-dannende enzym (EFE) reaktioner. Ny forskning beskriver de kemiske trin, som dette naturligt forekommende enzym bruger til at omdanne en almindelig kemisk forbindelse til eth
- Hvad har mindst masse i solsystemet?
- Billeder viser Lightsail 2-rumfartøjets solsejl er blevet indsat
- Hvad er to hovedafdelingen på jorden og forklarer den?
- At miste kystnære plantesamfund til klimaændringer vil svække havforsvaret
- Hvad er OKC's breddegrad og længdegrad?
- Hvad er sandt med alle makromolekyler?


