Lewis-struktur af N2H2Cl2:Trin-for-trin guide og forklaring
1. Tæl valenselektroner:
* Nitrogen (N) har hver 5 valenselektroner (2 N-atomer =10 elektroner)
* Brint (H) har 1 valenselektron hver (2 H-atomer =2 elektroner)
* Klor (Cl) har 7 valenselektroner hver (2 Cl-atomer =14 elektroner)
* Total valenselektroner =10 + 2 + 14 =26 elektroner
2. Centralatom:
* Nitrogen er det mindst elektronegative grundstof, så det vil være det centrale atom.
3. Enkeltobligationer:
* Forbind atomerne med enkeltbindinger.
* Dette bruger 6 elektroner (3 bindinger x 2 elektroner/binding).
4. Resterende elektroner:
* Du har 20 elektroner tilbage (26 - 6).
5. Fyld oktet for ydre atomer:
* Fuldfør oktetterne (8 elektroner) for brint- og kloratomerne ved at tilføje enlige par.
* Dette bruger 12 elektroner (2 H-atomer x 2 elektroner + 2 Cl-atomer x 3 elektroner).
6. Fyld oktet for centrale atomer:
* Nitrogenatomerne har nu 6 elektroner hver. Giv hvert nitrogenatom et ensomt par. Dette bruger de resterende 8 elektroner.
7. Tjek for formel debitering:
* Beregn den formelle ladning på hvert atom for at sikre, at strukturen er den mest stabile. Den formelle afgift skal være så tæt på nul som muligt.
* Formel ladning =(valenselektroner) - (ikke-bindende elektroner) - (1/2 bindingselektroner)
Lewis-struktur:
```
H Cl
\/
N-N
/ \
Cl H
```
Vigtige bemærkninger:
* Dette molekyle har resonansstrukturer, hvilket betyder, at dobbeltbindingen kan skifte mellem de to nitrogenatomer.
* Molekylet har en plan geometri.
* N-Cl-bindingerne er polære, og molekylet som helhed er også polært.
 Varme artikler
Varme artikler
-
 Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod
Nyt kompositmateriale, der kan køle sig selv ned under ekstreme temperaturerKredit:CC0 Public Domain Et banebrydende materiale, inspireret af naturen, der kan regulere sin egen temperatur og ligeså kunne bruges til at behandle forbrændinger og hjælpe rumkapsler til at mod -
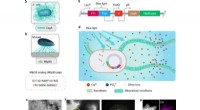 Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem
Lysfølsomme E. coli-funktionelle biofilm som stilladser til hydroxyapatitmineraliseringEngineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. Engineering light-responsive E. coli funktionelle biofilm som stilladser til HA-mineralisering. (a) Skem -
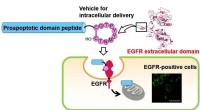 Opdagelsen af et nyt køretøjspeptid åbner en rute til levering af lægemidlerCyklisk decapeptid, som efterligner dimeriseringsarmen af EGF-receptoren (EGFR), blev tidligere fundet at være fanget i celler. Forfatterne har fundet det lovende potentiale for dette peptid som en
Opdagelsen af et nyt køretøjspeptid åbner en rute til levering af lægemidlerCyklisk decapeptid, som efterligner dimeriseringsarmen af EGF-receptoren (EGFR), blev tidligere fundet at være fanget i celler. Forfatterne har fundet det lovende potentiale for dette peptid som en -
 Kemisk syntese kunne producere mere potente antibiotikaKredit:CC0 Public Domain Ved at bruge en ny type kemisk reaktion, MIT-forskere har vist, at de kan modificere antibiotika på en måde, der potentielt kan gøre dem mere effektive mod lægemiddelresis
Kemisk syntese kunne producere mere potente antibiotikaKredit:CC0 Public Domain Ved at bruge en ny type kemisk reaktion, MIT-forskere har vist, at de kan modificere antibiotika på en måde, der potentielt kan gøre dem mere effektive mod lægemiddelresis
- Hvilke to store bestanddele udgør legeringen duralumin?
- Hvad er vigtigheden af temperaturregulerende mekanismer i organismer?
- Vandkølerdele kan være en kilde til eksponering for organofosfatester
- Kvinder bygger mindre effektive professionelle netværk end mænd, da de undervurderer selvværd
- Hvornår forventes vores sol at sprænge?
- At bygge havmure er et lille plaster på et gabende sår


