Hvad er definitionen af opløsning i kemi? – Forstå interaktioner mellem opløsningsmiddel og opløst stof
piyato/iStock/GettyImages
Hver gang du nipper til en sodavand, er du vidne til et klassisk eksempel på opløsning:en sødet drinksblanding bliver en homogen opløsning i kulsyreholdigt vand. Udtrykket opløse beskriver den proces, hvorved et opløsningsmiddel og et opløst stof kombineres for at danne en opløsning, uanset om stofferne er faste stoffer, væsker eller gasser.
Hvad vil det sige at opløses i kemi?
Opløsning sker, når molekylerne af et opløsningsmiddel og et opløst stof interagerer så stærkt, at det opløste stof bliver ensartet fordelt i hele opløsningsmidlet. Nogle stoffer opløses let i vand, men ikke i andre væsker, hvilket illustrerer, at både opløsningsmidlets og det opløste stofs molekylære egenskaber dikterer resultatet.
Hvad er opløselighed?
Opløselighed er et mål for, hvor meget af et stof, der kan opløses i en given mængde opløsningsmiddel ved en bestemt temperatur og tryk. Meget opløselige forbindelser, såsom natriumchlorid i vand, opløses fuldstændigt, hvorimod dårligt opløselige materialer kan tage lang tid eller slet ikke opløses. Vands polaritet – dets evne til at være vært for både positive og negative ladninger – gør det til det mest universelle opløsningsmiddel.
Hvad vil det sige at dissociere i kemi?
Dissociation refererer til adskillelsen af en ionforbindelse i dens bestanddele, når den opløses. I vandige opløsninger tiltrækker de polære ender af vandmolekyler kationer og anioner, der omgiver dem i en hydreringsskal og effektivt bryder iongitteret. Denne proces understøtter mange kemiske reaktioner, fra syre-base ligevægt til elektrolytledningsevne.
Mens olie og vand illustrerer et ikke-dissocierende system – oliens upolære molekyler og vands polære molekyler blandes ikke godt – er dissociationsprincippet fortsat centralt for at forstå, hvordan elektrolytter opfører sig i opløsning.
 Varme artikler
Varme artikler
-
 Et smertefrit klæbemiddel:Klæbemidler til biomedicinske applikationer kan løsnes med lysDisse to hydrogeler, klæbet med en vandig opløsning af polymerkæder, adskilles let i nærværelse af UV -lys. Kredit:Image/Zhigang Suo/Harvard SEAS Afbrydelse af en plaster kan snart blive meget min
Et smertefrit klæbemiddel:Klæbemidler til biomedicinske applikationer kan løsnes med lysDisse to hydrogeler, klæbet med en vandig opløsning af polymerkæder, adskilles let i nærværelse af UV -lys. Kredit:Image/Zhigang Suo/Harvard SEAS Afbrydelse af en plaster kan snart blive meget min -
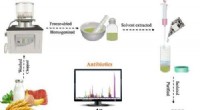 Registrering af spormængder af flere klasser af antibiotika i fødevarerKredit:American Chemical Society Udbredt brug af antibiotika i menneskers sundhedspleje og husdyrhold har ført til, at spormængder af stofferne ender i fødevarer. Langtidsforbrug kan forårsage sun
Registrering af spormængder af flere klasser af antibiotika i fødevarerKredit:American Chemical Society Udbredt brug af antibiotika i menneskers sundhedspleje og husdyrhold har ført til, at spormængder af stofferne ender i fødevarer. Langtidsforbrug kan forårsage sun -
 Oprydning af brintoverilteproduktionSolugens proprietære proces til fremstilling af hydrogenperoxid bruger modificerede enzymer og billige forbindelser som sukker. Det bliver i øjeblikket brugt i to pilotanlæg, der producerer mere end 1
Oprydning af brintoverilteproduktionSolugens proprietære proces til fremstilling af hydrogenperoxid bruger modificerede enzymer og billige forbindelser som sukker. Det bliver i øjeblikket brugt i to pilotanlæg, der producerer mere end 1 -
 RNA grundlæggende byggesten produceret biokatalytisk for første gangGraz-forskerne er de første i verden til at demonstrere YeiN, et enzym, der er en egnet biokatalysator til fremstilling af C-nukleosider, de grundlæggende byggesten i RNA. Kredit:Lunghammer - TU Graz
RNA grundlæggende byggesten produceret biokatalytisk for første gangGraz-forskerne er de første i verden til at demonstrere YeiN, et enzym, der er en egnet biokatalysator til fremstilling af C-nukleosider, de grundlæggende byggesten i RNA. Kredit:Lunghammer - TU Graz
- Hvordan fjernes vestigiale strukturer ikke ved naturlig selektion?
- Hvorfor føler vi ikke varmen og lyset fra stjerner, selvom de er så store varme?
- Ikke alle drikkevandsfiltre i hjemmet fjerner giftigt PFAS fuldstændigt
- Hvilket fast stof er lettere end vand, men tungere olie?
- Hvad hedder hvide blodlegemer, der kan indhylles patogener?
- Sådan bestemmes Shock Spring Rate


