Beregning af ækvivalente enheder i kemi:en praktisk vejledning
Af Rosann Kozlowski | Opdateret 30. august 2022
Foto:Photongpix/iStock/GettyImages
I kemi hjælper konceptet med ækvivalente enheder - eller ækvivalenter - med at kvantificere den reaktive kapacitet af arter såsom elektroner eller ioner. En ækvivalent repræsenterer antallet af elektroner eller ioner, som et stof kan donere eller acceptere i en given reaktion.
Hvad er ækvivalenter?
En arts reaktive kapacitet afhænger af, hvad der overføres under en kemisk reaktion. I syre-base kemi er en ækvivalent lig med mængden af et stof, der reagerer med et mol hydrogenioner (H⁺). I redoxreaktioner er det et mol elektroner.
Knytter oxidationstilstand til ækvivalenter
Et grundstofs oxidations- (eller valenstilstand) angiver, hvor mange elektroner der er involveret i dets interaktioner. Derfor er antallet af ækvivalenter ofte lig med den absolutte værdi af oxidationstilstanden.
- Calciumion (Ca²⁺) – 2 ækvivalenter
- Aluminiumion (Al³⁺) – 3 ækvivalenter
Ækvivalenter i syrer og baser
For syrer svarer en ækvivalent til antallet af brintioner et molekyle kan donere. Dette tal er simpelthen koefficienten for brint i molekylformlen.
- Saltsyre (HCl) – 1 ækvivalent
- Svovlsyre (H₂SO₄) – 2 ækvivalenter
- Phosphorsyre (H₃PO₄) – 3 ækvivalenter
- Salpetersyre (HNO₃) – 1 ækvivalent
For baser er ækvivalenten antallet af hydroxidioner (OH⁻), de giver:
- Natriumhydroxid (NaOH) – 1 ækvivalent
- Bariumhydroxid (Ba(OH)₂) – 2 ækvivalenter
Vurdering af syre-base-styrke med ækvivalenter
En ækvivalent af en syre reagerer med en ækvivalent af en base. Således giver lige ækvivalenter af en syre og en base en neutral opløsning. For eksempel neutraliserer 1 ækvivalent HCl 1 ækvivalent NaOH, mens 2 ækvivalenter H2SO4 kræver den dobbelte mængde NaOH.
Praktiske anvendelser af ækvivalenter
Selvom moderne laboratorier sjældent bruger ækvivalenter til rutineberegninger, er de stadig vigtige for at bestemme gramækvivalent vægt og normalitet, især i titreringer.
Gram-ækvivalent vægtberegninger
Den gramækvivalente vægt af en syre eller base beregnes som:
Ækvivalentvægt =Molekylvægt ÷ antal ækvivalenter
Eksempel: Find gramækvivalentvægten af phosphorsyre (H₃PO₄).
- Beregn dens molekylvægt:3(1,01) + 30,97 + 4(16,00) =127gmol⁻¹.
- Antal ækvivalenter (n) =3.
- Ækvivalent vægt =127 ÷ 3 =42,3geq⁻¹.
Normalitetsberegninger
Normalitet (N) er defineret som ækvivalenter pr. liter opløsning. Formlen er:
N =(masse af opløst stof ÷ ækvivalentvægt) ÷ volumen inL
Eksempel: Forbered en 2N opløsning af H₃PO4.
- Ønsket normalitet:N=2eqL⁻¹.
- Lydstyrke:V=1L.
- Tilsvarende vægt:42,3geq⁻¹.
- Påkrævet masse:m =N × V × ækvivalentvægt =2 × 1 × 42,3 =84,6 g.
Opløs således 84,6 g phosphorsyre i vand nok til at nå 1 L for at opnå en 2N opløsning.
Vigtige ting
- Ækvivalenter giver en bekvem måde at relatere støkiometri til reaktiv kapacitet.
- De er afgørende for beregning af gramækvivalent vægt og normalitet i titreringsarbejde.
- Forståelse af ækvivalenter bygger bro mellem begreber inden for syre-base og redoxkemi.
 Varme artikler
Varme artikler
-
 Hvidløg og fluor kombination viser lovende som lægemiddelbehandlingKunne kombinationen af hvidløg og fluor være fremtiden for lægemiddelterapi? Kredit:University at Albany Der er meget mere ved hvidløg end dens karakteristiske lugt og stærke, skarp smag. I årh
Hvidløg og fluor kombination viser lovende som lægemiddelbehandlingKunne kombinationen af hvidløg og fluor være fremtiden for lægemiddelterapi? Kredit:University at Albany Der er meget mere ved hvidløg end dens karakteristiske lugt og stærke, skarp smag. I årh -
 Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m
Variabel valens:Hvordan elementer ændrer deres ladningstilstande i kemiAf David Stewart • Opdateret 24. marts 2022 Elektroner kredser om en atomkerne i diskrete energiniveauer. De yderste elektroner - kendt som valenselektroner - bestemmer, hvordan et atom interagerer m -
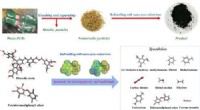 Mod sikrere bortskaffelse af printkortKredit:American Chemical Society Printplader er vitale komponenter i moderne elektronik. Imidlertid, når de har tjent deres formål, de bliver ofte brændt eller begravet på lossepladser, forurener
Mod sikrere bortskaffelse af printkortKredit:American Chemical Society Printplader er vitale komponenter i moderne elektronik. Imidlertid, når de har tjent deres formål, de bliver ofte brændt eller begravet på lossepladser, forurener -
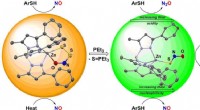 Sporing af nitrogenoxid-signalvejenKredit:Wiley Både nitrogenoxid (NO) og svovlbrinte (H 2 S) fungerer som gasformige signalmolekyler med lignende fysiologiske virkninger. Mange af de kritiske spørgsmål om samspillet mellem disse
Sporing af nitrogenoxid-signalvejenKredit:Wiley Både nitrogenoxid (NO) og svovlbrinte (H 2 S) fungerer som gasformige signalmolekyler med lignende fysiologiske virkninger. Mange af de kritiske spørgsmål om samspillet mellem disse
- Måling af pesticidmængden alene afgør ikke risikoen
- Hvorfor er enzymer så specifikke i deres handlinger?
- Hvad repræsenterer Oceanic Ridge Systems?
- Billige forårstrøfler eller udsøgte Piemonte-trøfler? Ny analysemetode kan afsløre fødevaresvi…
- Uralbjergene, der er dannet som et resultat af kollisionen Europa med Asien Ural, er derfor mest san…
- Hvordan kan du se en genstand, der ikke udsender lys?


