Hvordan atomradius former reaktiviteten af halogener
Ryan McVay/Photodisc/Getty Images
Halogenerne – fluor, klor, brom, jod og astatin – optager gruppe 17 i det periodiske system. Med syv valenselektroner er de meget ivrige efter at acceptere en ekstra elektron og opnå en stabil oktet. Dette drev understøtter deres intense reaktivitet, som spænder over faste, flydende og gasfaser under standardbetingelser.
Halogens' jagt på en oktet
Hvert atom stræber efter otte elektroner i sin valensskal. Halogener, der kun sidder en elektron kort, accepterer let elektroner, hvilket gør dem til blandt de mest reaktive grundstoffer i det periodiske system.
Atomradius' rolle
Størrelsen af et atoms kerne i forhold til dets elektronsky - dets atomradius - bestemmer, hvor stærkt kernen tiltrækker elektroner. I mindre halogenatomer er kernen tættere på valenselektronerne, hvilket øger det elektrostatiske træk og accelererer erhvervelsen af en ekstra elektron. Følgelig udviser fluor med den mindste radius den højeste reaktivitet, efterfulgt af klor, brom, jod og astatin.
George Doyle/Stockbyte/Getty Images
Jason Reed/Photodisc/Getty Images
 Varme artikler
Varme artikler
-
 Beregning af volumen af en firkantet pyramide:Trin-for-trin-vejledningBesjunior/iStock/GettyImages Volumenet af et fast stof er det tredimensionelle rum, det optager, hvilket også kan ses som kapaciteten til at indeholde en væske eller gas. For en kvadratisk pyramide –
Beregning af volumen af en firkantet pyramide:Trin-for-trin-vejledningBesjunior/iStock/GettyImages Volumenet af et fast stof er det tredimensionelle rum, det optager, hvilket også kan ses som kapaciteten til at indeholde en væske eller gas. For en kvadratisk pyramide – -
 Konvertering af Fahrenheit til Kelvin:En klar trin-for-trin guideAf Kate Bruscke Opdateret 30. august 2022 Nøjagtig temperaturkonvertering er en grundlæggende færdighed for forskere inden for geovidenskab, kemi og fysik. Kelvin, opkaldt efter den skotske videnska
Konvertering af Fahrenheit til Kelvin:En klar trin-for-trin guideAf Kate Bruscke Opdateret 30. august 2022 Nøjagtig temperaturkonvertering er en grundlæggende færdighed for forskere inden for geovidenskab, kemi og fysik. Kelvin, opkaldt efter den skotske videnska -
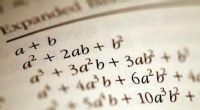 Identifikation af primære polynomier i algebra:en trin-for-trin guideAf bidragyder Opdateret 30. august 2022 I algebra er et primtpolynomium (også kaldet et irreducerbart polynomium) kan ikke faktoriseres yderligere over hele tallene. Det er vigtigt at genkende disse
Identifikation af primære polynomier i algebra:en trin-for-trin guideAf bidragyder Opdateret 30. august 2022 I algebra er et primtpolynomium (også kaldet et irreducerbart polynomium) kan ikke faktoriseres yderligere over hele tallene. Det er vigtigt at genkende disse -
 Mestring af sandsynlighedsberegninger for terninger:En trin-for-trin guideFlavio Coelho/Getty Images Uanset om du er nysgerrig efter dine odds i et spil eller forbereder dig til en sandsynlighedseksamen, er det at mestre terningesandsynligheder et solidt fundament. Det int
Mestring af sandsynlighedsberegninger for terninger:En trin-for-trin guideFlavio Coelho/Getty Images Uanset om du er nysgerrig efter dine odds i et spil eller forbereder dig til en sandsynlighedseksamen, er det at mestre terningesandsynligheder et solidt fundament. Det int
- Hvad betyder volumen, når du taler om fysiske egenskaber?
- Hvad er et evolutionært spor?
- Sådan fungerer gasturbinemotorer
- Hvad er den kemiske sammensætning af phenyl?
- Forskere til at undersøge tørketolerante vinstokke
- En chance for Pluto-krammerne? Videnskabsmand leder indsatsen for at genoprette underdogs planetaris…


