Ny undersøgelse giver forskere mulighed for at teste terapeutiske midler for sjælden neurodegenerativ sygdom, der rammer små børn
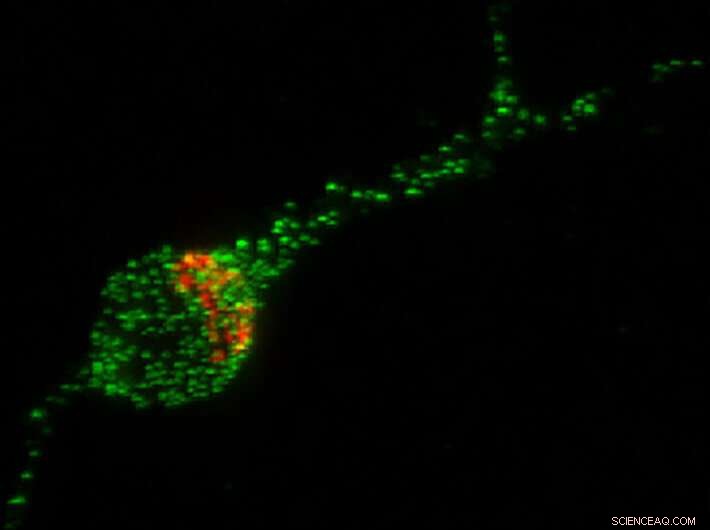
I dette billede af en human STEM-celle-afledt neuron er Trk-fusioneret genprotein (TFG) vist med grønt, og Golgi Apparatus, organellen som hjælper med at pakke proteiner til transport til resten af kroppen, er vist med rødt. Kredit:University of Wisconsin-Madison
For første gang vil forskere være i stand til at teste terapeutiske midler til en gruppe af sjældne neurodegenerative sygdomme, der påvirker spædbørn og småbørn, takket være en ny forskningsmodel skabt af forskere ved University of Wisconsin-Madison. Deres resultater er offentliggjort i Proceedings of the National Academy of Sciences .
Arvelige spastiske paraplegier (HSP'er) er en gruppe af neurodegenerative sygdomme forårsaget af genetiske mutationer. De får titusindvis af børn til at udvikle øget muskeltonus i deres underekstremiteter, hvilket forårsager svaghed i deres ben og i sidste ende påvirker deres evne til at kravle eller gå.
"Børn så tidligt som seks måneders alderen, der har disse mutationer, begynder at vise tegn på sygdom," siger Anjon Audhya, professor ved Institut for Biomolekylær Kemi ved UW-Madison. "Mellem to og fem år bliver disse børn kørestolsbundne, og de vil desværre aldrig kunne gå."
Audhya forklarer, at mange videnskabsmænd ikke har forsket i spastiske paraplegier, fordi der ikke har været en god model til at studere sygdommens oprindelse eller teste terapeutika. Tidligere musemodeller har ikke fungeret, fordi de neuronale baner, der bærer bevægelsesrelateret information i hele kroppen, ser ud til at være for forskellige fra dem hos mennesker, og forskere har endnu ikke forfulgt kliniske forsøg med mennesker.
Audhya arbejdede sammen med et tværfagligt team af UW-Madison-forskere for at studere en specifik mutation, der forårsager HSP hos små børn. De brugte derefter det, de lærte, til at skabe en bedre model – hos rotter.
Mutationen, som forskerne valgte, virker på et protein kaldet Trk-fusioneret gen eller TFG. Sunde TFG-proteiner arbejder inde i nerveceller, eller neuroner, for at transportere andre proteiner fra en del af cellen til en anden. En neurons opgave er at transportere meddelelser i form af elektriske signaler mellem hjernen og resten af kroppen.
De proteiner, der er afhængige af TFG for deres transport, holder disse neuronale veje sunde, og hjælper med at styre, hvilke elektriske signaler hjernen sender til kroppen, og hvilke signaler der skal hæmmes. Ved at afbalancere de rigtige stimuleringsniveauer kan neuroner styre bevægelser som f.eks. at trække benmusklerne, der er involveret i gang, sammen.
Hos små børn med en mutation på deres TFG-gen bevæger neuronale proteiner sig ikke effektivt gennem deres nerveceller. Audhya siger, at dette kan skabe en ubalance af elektrisk stimulation, der gør det muligt at sende en overflod af elektriske signaler til underekstremiteterne, hvilket resulterer i forhøjet muskeltonus. Over tid fører den overdrevne muskeltonus til et tab af motorisk funktion.
"Du kan forestille dig, at hvis du strækker dit ben rigtig hårdt ud, og du bruger al din energi på at bøje den muskel, er det virkelig svært at bevæge den," siger Audhya, der også er seniordekan for grundforskning, bioteknologi og kandidatstudier i UW School of Medicine and Public Health.
Forskerne søgte efter en brugbar model og henvendte sig til rotter for at hjælpe disse børn. Holdet brugte CRISPR-genredigeringsteknologi til at skabe de mutationer i rotteembryoner, der fører til HSP. Dette gjorde det muligt for dem at studere, hvordan sygdommen udvikler sig fra tidlig udvikling og overvåge udviklingen af symptomer efter fødslen.
Ikke alene er rotternes neuronale veje tættere på menneskers, men forskerne så, at symptomer udviklede sig på samme måde hos rotter som dem, der ses hos børn med HSP. Det skete også på en tilstrækkelig hurtig tidsskala til, at videnskabsmænd nemt skulle være i stand til at teste levedygtigheden af potentielle lægemidler.
"Motion har været den eneste terapi, der findes for disse patienter, og det er virkelig utilfredsstillende," siger Audhya. "Jeg synes, vi har taget et stort spring fremad ved blot at have en model, hvor man kan teste forskellige hypoteser. Det er stort set fra mit perspektiv."
De indviklede detaljer, der er involveret i biomolekylær kemi, kan virke hverdagsagtige for nogle, men grundlæggende videnskab som denne fascinerer Audhya. Det var først, da han tog kontakt med patienter, der har HSP, at han fuldt ud forstod den potentielle indvirkning, hans arbejde kunne have.
"Det er befolkninger, der er underbetjent. En farmavirksomhed vil sandsynligvis ikke bruge enorme ressourcer til en ramt befolkning, der er så lille. I stedet vil de fokusere på sygdomme som Alzheimers og Parkinsons," siger han. "Så jeg følte, at her er en sygdom, der er bredt overset, underinvesteret i, og her er et område, hvor vi kan gøre en indflydelse."
Audhya sagde, at han håber, at denne nye model vil inspirere flere videnskabsmænd til at studere HSP'er for at forbedre forståelsen af sygdommens udvikling og til sidst forbedre adgangen til terapeutiske midler, der vil hjælpe børn, der lever med den. + Udforsk yderligere
Genmutationer fra patienter med invaliderende anfald og bevægelsesforstyrrelser skabt i mus
 Varme artikler
Varme artikler
-
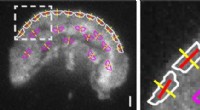 Interne kræfter, der styrer cellemigration, afsløres ved levende cellemikroskopiOrientering af integriner i forkant af en migrerende Jurkat T -celle, analyseret ved hjælp af et fluorescenspolariseret lysmikroskop (øjeblikkeligt FluoPolScope) udviklet på Marine Biological Laborato
Interne kræfter, der styrer cellemigration, afsløres ved levende cellemikroskopiOrientering af integriner i forkant af en migrerende Jurkat T -celle, analyseret ved hjælp af et fluorescenspolariseret lysmikroskop (øjeblikkeligt FluoPolScope) udviklet på Marine Biological Laborato -
 Genetisk variabilitet understøtter planters overlevelse under tørkeSennepskarse, Arabidopsis thaliana, vokser på en sandstrand ved Østersøen i det sydlige Sverige. Kredit:MPI f. Udviklingsbiologi/ M. Exposito-Alonso I den første undersøgelse for at forudsige, om
Genetisk variabilitet understøtter planters overlevelse under tørkeSennepskarse, Arabidopsis thaliana, vokser på en sandstrand ved Østersøen i det sydlige Sverige. Kredit:MPI f. Udviklingsbiologi/ M. Exposito-Alonso I den første undersøgelse for at forudsige, om -
 Hvordan bier finder vej hjemHonningbi (Apis mellifera) lander på en marietidselblomst (Silybum marianum). Kredit:Fir0002/Flagstaffotos/ Wikipedia/GFDL v1.2 Hvordan kan en bi flyve direkte hjem midt om natten efter en komplic
Hvordan bier finder vej hjemHonningbi (Apis mellifera) lander på en marietidselblomst (Silybum marianum). Kredit:Fir0002/Flagstaffotos/ Wikipedia/GFDL v1.2 Hvordan kan en bi flyve direkte hjem midt om natten efter en komplic -
 Ikke så kold and? Mennesket bliver ved med at lede efter uddøde fugleDette foto fra oktober 2017 leveret af Cornell University Museum of Vertebrates viser et eksemplar af en pink-headed and i Ithaca, N.Y. På grund af prøvens alder, hovedet har skiftet farve. I oktober
Ikke så kold and? Mennesket bliver ved med at lede efter uddøde fugleDette foto fra oktober 2017 leveret af Cornell University Museum of Vertebrates viser et eksemplar af en pink-headed and i Ithaca, N.Y. På grund af prøvens alder, hovedet har skiftet farve. I oktober
- Pærer i trådkorset for Trump-administrationens miljøtilbagetrækninger
- Hvad er fusion af to gameter til dannelse af en diploid zygote?
- Forskere simulerer det intracellulære miljø i en selvlysende bakteriecelle
- Tabt generation? Krisen i 2008 tynger stadig Millennials
- Hvor skal man placere et system til høst af regnvand
- Søgeresultater, der ikke er forudindtaget langs partilinjer, Stanford undersøgelse finder


