Lysshow i levende celler:Ny metode tillader samtidig fluorescerende mærkning af mange proteiner
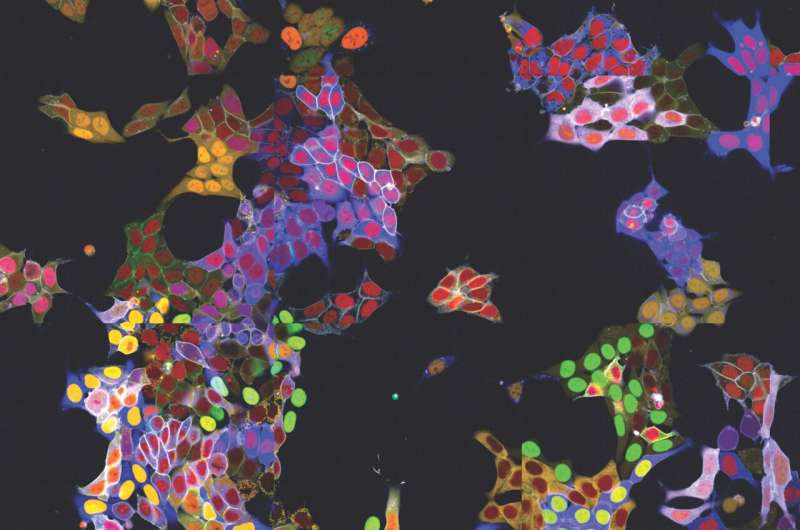
At observere proteiner præcist inde i celler er ekstremt vigtigt for mange forskningsgrene, men det har været en betydelig teknisk udfordring – især i levende celler, da den nødvendige fluorescerende mærkning skulle fastgøres individuelt til hvert protein.
Forskergruppen ledet af Stefan Kubicek ved CeMM har nu overvundet denne hindring:Med en metode kaldet "vpCells" er det muligt at mærke mange proteiner samtidigt ved hjælp af fem forskellige fluorescerende farver. Denne automatiserede high-throughput tilgang, hjulpet af AI-assisteret billedgenkendelse, åbner op for helt nye applikationer inden for forskellige discipliner, fra fundamental cellebiologi til lægemiddelopdagelse. Studiet er blevet publiceret i tidsskriftet Nature Cell Biology .
Uden proteiner ville livet, som vi kender det, være utænkeligt. De giver den strukturelle ramme for celler, fungerer som enzymer til at kontrollere stofskiftet og gør det muligt for celler at kommunikere med deres miljø som membranreceptorer, transportører eller signalmolekyler. Alle disse funktioner kan kun opfyldes, hvis proteinerne er placeret det rigtige sted i cellen. Ofte ændrer selv et proteins egenskaber sig, når det ændrer sin placering - kontrol over dets lokalisering i cellen betyder derfor også kontrol over dets funktion.
For at forstå og udforske funktionen af proteiner er det vigtigt præcist at bestemme og spore deres placering i cellen. Proteiner pendler ofte dynamisk mellem forskellige organeller og rum i cellen. For at visualisere dem under mikroskopet er de ofte forbundet med en fluorescerende, stærkt skinnende proteinkomponent. Denne metode har imidlertid været udsat for tekniske vanskeligheder:Typisk kunne den fluorescerende komponent kun bindes til ét protein ad gangen, og for at mærke flere proteiner skulle celler normalt dræbes og fikseres.
Den nye metode præsenteret af Stefan Kubiceks gruppe, kaldet "visual proteomics Cells" (forkortet vpCells), tillader proteiner at blive fluorescerende mærket på en måde, der bevarer deres endogene reguleringsmekanismer. I stedet for at mærke ét protein ad gangen, kan vpCells fusionere mange proteiner samtidigt med et fluorescerende tag i en såkaldt multiplex-tilgang.
En forløber for denne metode blev allerede beskrevet af Kubiceks team i 2020 for at studere metaboliske enzymer. Nu er det blevet udvidet og forbedret på tre måder:
For det første kan vpCells mærke alle teoretisk mulige proteiner ved hjælp af CRISPR/Cas9-genredigeringsværktøjet til genetisk at vedhæfte fluorescerende proteiner til proteinerne under undersøgelse. Kubiceks gruppe har skabt et "bibliotek" i hele genomet til dette formål, hvilket muliggør fluorescerende mærkning og systematisk funktionel udforskning af alle mulige humane proteiner.
For det andet bruger vpCells ikke kun én fluorescerende farve, men i alt fem komplementære farver. I hver celle er to forskellige proteiner, der skal spores, markeret. Derudover bruges en anden farvemarkering til bedre at skelne individuelle kloner. Og yderligere to farver markerer cellekernen og membranen for at afgrænse individuelle celler bedre.
For det tredje gør dette farveskema ikke kun muligt at generere visuelt tiltalende billeder, men også at optisk genkende og skelne mellem de forskellige proteiner. Normalt kræver dette kompleks DNA-sekventering efter billeddannelse for at bestemme, hvilket protein der er mærket. vpCells-tilgangen på den anden side gør det muligt at træne et AI-assisteret billedgenkendelsessystem til at genkende, hvilket protein der er markeret i hvilken celle, udelukkende baseret på fluorescensmikroskopibilleder.
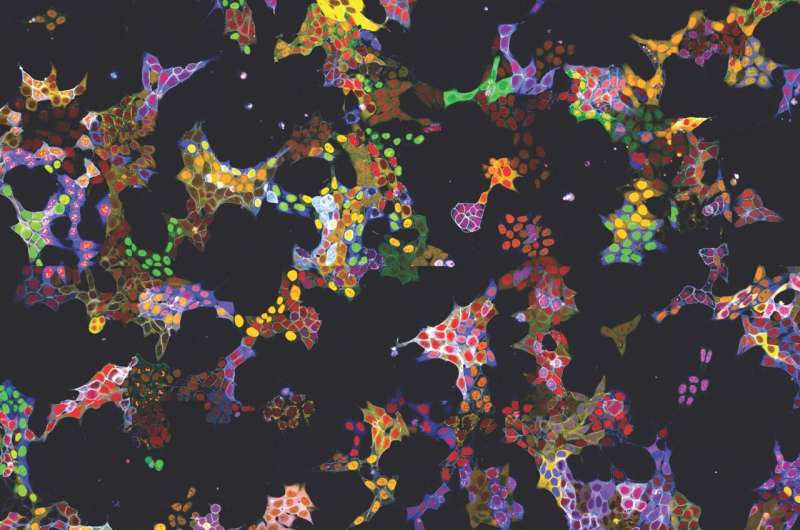
Metoden har allerede vist sin anvendelighed i to anvendelser:På den ene side blev mere end 4.500 cellelinjer genereret som reportere for mere end 1.100 proteiner. Disse cellelinjer blev brugt til at træne AI-modellerne og til at beskrive lokalisering af proteinerne i deres basale tilstand. Alle billeder af de individuelle mærkede proteiner er tilgængelige på den offentligt tilgængelige webdatabase vpCells.
På den anden side blev de levende reporterceller brugt til et specifikt forskningsspørgsmål:Kubiceks team undersøgte effekten af mere end 1000 småmolekylære stoffer på 61 proteiner, der er relevante for kræftceller. Forskerne fandt ud af, at 44 af de testede stoffer ændrede mængden eller lokaliseringen af individuelle proteiner inden for 6 timer. Et af stofferne viste sig at være en hæmmer af proteintransport fra cellekernen, som har en lignende effekt som et klinisk godkendt lægemiddel mod myelomatose, en kræftsygdom i det bloddannende system.
"Disse resultater giver et første indblik i vpCells-metodens alsidighed," siger Kubicek. "Vi forventer mange flere fremtidige anvendelser, fra fundamental cellebiologi til anvendt lægemiddelopdagelse."
Flere oplysninger: Poolet flerfarvet tagging til visualisering af subcellulær proteindynamik, Nature Cell Biology (2024). DOI:10.1038/s41556-024-01407-w
Journaloplysninger: Naturcellebiologi
Leveret af CeMM Research Center for Molecular Medicine ved det østrigske videnskabsakademi
 Varme artikler
Varme artikler
-
 Højteknologiske værktøjer afslører opaliseret fossilt skeletEn rekonstruktion af, hvordan denne lille dinosaur kan have set ud. Kredit:James McKinnon Palæontologer fra Flinders University bruger en mikro-CT-scanner og 3D-print til at rekonstruere en lille d
Højteknologiske værktøjer afslører opaliseret fossilt skeletEn rekonstruktion af, hvordan denne lille dinosaur kan have set ud. Kredit:James McKinnon Palæontologer fra Flinders University bruger en mikro-CT-scanner og 3D-print til at rekonstruere en lille d -
 Uventet regulering af transkriptionsfaktorer, der er kritiske for udviklingI et nyt blad, forskerholdet af Hélene Cousin og Dominique Alfandari ved UMass Amherst beskriver for første gang, hvordan to transkriptionsfaktorer, der er absolut essentielle for menneskelig udviklin
Uventet regulering af transkriptionsfaktorer, der er kritiske for udviklingI et nyt blad, forskerholdet af Hélene Cousin og Dominique Alfandari ved UMass Amherst beskriver for første gang, hvordan to transkriptionsfaktorer, der er absolut essentielle for menneskelig udviklin -
 Et våbenkapløb om madspild:Sydney kakaduer åbner stadig skraldespande ved kantstenen, på trods a…Kredit:Barbara Klump, Forfatter leveret Hold da kæft! Kakaduen har lige åbnet min skraldespand, og den spiser min resterende pizza. Det kan vi ikke have, jeg sætter en sten på låget for at forhindr
Et våbenkapløb om madspild:Sydney kakaduer åbner stadig skraldespande ved kantstenen, på trods a…Kredit:Barbara Klump, Forfatter leveret Hold da kæft! Kakaduen har lige åbnet min skraldespand, og den spiser min resterende pizza. Det kan vi ikke have, jeg sætter en sten på låget for at forhindr -
 Global undersøgelse afslører en betydelig nettorisiko for sjældne, skattet NZ pingvinGuløjet pingvin, der døde som bifangst i et netsæt til skolehaj og rig påsat. Kredit:University of Otago En ny anmeldelse, hvis forfattere omfatter forskere fra University of Otago, fremhæver den
Global undersøgelse afslører en betydelig nettorisiko for sjældne, skattet NZ pingvinGuløjet pingvin, der døde som bifangst i et netsæt til skolehaj og rig påsat. Kredit:University of Otago En ny anmeldelse, hvis forfattere omfatter forskere fra University of Otago, fremhæver den
- Hvad er processen med at forbinde små molekyler sammen for at danne lange kæder kaldet?
- Måne kort, månens oprindelse og alt derimellem
- Hvor længe varer førskolefordelen?
- Undersøg først for at forbinde ukrudtsmiddel Roundup til kramper hos dyr
- Du kører som en pige:Undersøgelse viser kønsbias i opfattelsen af samkørsel
- Underwater Lost City blev ikke bygget af mennesker,


