Hvad er de 7 diatomiske grundstoffer?
Diatomiske elementer hader at være alene - så meget, at de bare ikke findes som enkelte atomer.
I stedet er de altid to atomer af det samme rene grundstof bundet sammen. Det er lige i navnet:Di - betyder "to" og atomare betyder "af atomerne". Og elementer er universets grundlæggende byggesten.
Men ud af hele det periodiske system er der kun syv diatomiske grundstoffer:
- Brint H2
- Nitrogen N2
- Fluor F2
- Oxygen O2
- Jod I2
- Klor Cl2
- Brom Br2
Hvorfor kun syv?
Der er egentlig kun syv diatomiske grundstoffer. Fem af dem - brint, nitrogen, fluor, oxygen og klor - er gasser ved stuetemperatur og normalt tryk. De kaldes nogle gange elementære gasser. Brom er altid en væske, mens jod kan være en væske eller fast, når det er ved stuetemperatur, afhængigt af en række faktorer. Alle syv er ikke-metalliske.
Andre elementer kan selvfølgelig binde sammen; de kaldes diatomiske molekyler . Sådan får vi bordsalt (natrium + klor =NaCl, natriumklorid). Diatomiske molekyler som dette findes overalt. Nogle andre grundstoffer kan danne diatomiske molekyler, men bindingerne er meget svage og ustabile. De forbliver ikke diatomiske i lang tid. Kun disse syv diatomiske grundstoffer danner stærke bindinger og findes næsten altid i denne form.
Dermed ikke sagt, at diatomiske elementer er sjældne - tværtimod! Nitrogen og oxygen, i deres diatomiske former N2 og O2 , udgør 99 procent af Jordens atmosfære. Det er det modsatte af sjældent.
Har du brug for en nem måde at huske disse syv på? Prøv denne mnemonic:H ave N o F øre O f I ce C gamle B eer. Det første bogstav i hvert ord vil minde dig om hvert diatomisk element.
Nu er det elementærtGrundstoffer kan også være monoatomiske, hvilket betyder, at der kun er ét atom. (Mon- betyder "én.") Helium er et monoatomisk grundstof. Og oxygen kan være triatomisk, med tre atomer bundet sammen. Det er det, vi almindeligvis kalder "ozon."
 Varme artikler
Varme artikler
-
 Materiale, der holder ting koldt og varmtVarme er overførsel af energi fra et højtemperaturlegeme til et lavere temperaturlegeme og er en grundlæggende mængde i fysik. Et materiale, der forhindrer overførsel af varme er kendt som en varmeiso
Materiale, der holder ting koldt og varmtVarme er overførsel af energi fra et højtemperaturlegeme til et lavere temperaturlegeme og er en grundlæggende mængde i fysik. Et materiale, der forhindrer overførsel af varme er kendt som en varmeiso -
 Quantum computing i stor skala:Forskere opnår kompakte, følsom qubit -aflæsningForfatterne til papiret, fra venstre mod højre:ph.d. elev Mark R. Hogg; Professor Michelle Simmons; Post Doc Matthew G. House; Ph.d. studerende Prasanna Pakkiam; Post Doc Andrey Timofeev. Kredit:UNSW
Quantum computing i stor skala:Forskere opnår kompakte, følsom qubit -aflæsningForfatterne til papiret, fra venstre mod højre:ph.d. elev Mark R. Hogg; Professor Michelle Simmons; Post Doc Matthew G. House; Ph.d. studerende Prasanna Pakkiam; Post Doc Andrey Timofeev. Kredit:UNSW -
 Ny undersøgelse kaster lys over, hvordan ultralavfrekvente radiobølger og plasma interagererForskere ved University of California, Los Angeles præsenterer forskning i et mærkeligt kosmisk fænomen kendt som whistlers - meget lavfrekvente pakker af radiobølger, der løber langs magnetiske feltl
Ny undersøgelse kaster lys over, hvordan ultralavfrekvente radiobølger og plasma interagererForskere ved University of California, Los Angeles præsenterer forskning i et mærkeligt kosmisk fænomen kendt som whistlers - meget lavfrekvente pakker af radiobølger, der løber langs magnetiske feltl -
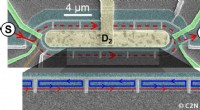 Makroskopisk elektron-kvantesammenhæng i et kredsløb i fast tilstandFarvet scanningselektronmikrograf af prøven:Mach Zehnder interferometer og indespærringsstrategi, der bruges til at opnå og demonstrere en rekordelektronisk kohærenslængde på 0,25 mm. Kredit:© C2N
Makroskopisk elektron-kvantesammenhæng i et kredsløb i fast tilstandFarvet scanningselektronmikrograf af prøven:Mach Zehnder interferometer og indespærringsstrategi, der bruges til at opnå og demonstrere en rekordelektronisk kohærenslængde på 0,25 mm. Kredit:© C2N
- Afghanistan har enorme mineralrigdomme, men står over for stejle udfordringer for at udnytte den
- Transaktionsgebyrer ændrer bitcoins kultur, siger undersøgelse
- Nanopartikler bruges til at transportere kræftbekæmpende midler til celler
- Hvorfor voldtægtsofre så ofte bliver overladt til at løse deres egne sager
- For at forudsige fremtiden for polarisen, miljøforskere ser på fortiden
- Storme forhåndsviser havstigningsskader på byer i Californien, veje


